Формула гистидина: Атлас аминокислот: гистидин
Гистидин — описание вещества, фармакология, применение, противопоказания, формула
Содержание
- Структурная формула
- Русское название
- Английское название
- Латинское название вещества Гистидин
- Химическое название
- Брутто формула
- Фармакологическая группа вещества Гистидин
- Нозологическая классификация
- Код CAS
- Фармакологическое действие
- Характеристика
- Фармакология
- Применение вещества Гистидин
- Противопоказания
- Побочные действия вещества Гистидин
- Передозировка
- Способ применения и дозы
Структурная формула
Русское название
Гистидин
Английское название
Histidine
Латинское название вещества Гистидин
Histidinum (род. Histidini)
Histidini)
Химическое название
L-Гистидин (и в виде гидрохлорида или аскорбата)
Брутто формула
C6H9N3O2
Фармакологическая группа вещества Гистидин
Белки и аминокислоты
Нозологическая классификация
Список кодов МКБ-10
- I70 Атеросклероз
- B19 Вирусный гепатит неуточненный
Код CAS
71-00-1
Фармакологическое действие
Фармакологическое действие —
антиатеросклеротическое, гиполипидемическое.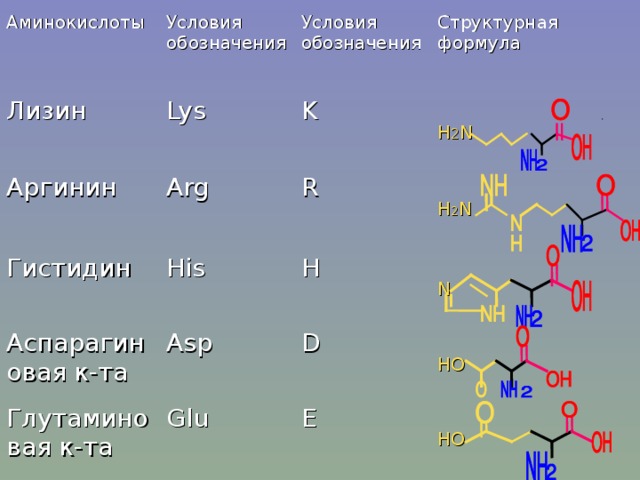
Характеристика
Прозрачные бесцветные кристаллы или белый кристаллический порошок слабокислого вкуса. Растворим в воде, очень мало — в этаноле.
Фармакология
Незаменимая аминокислота. В организме подвергается декарбоксилированию с образованием гистамина. Вызывает спазм гладкой мускулатуры бронхов и ЖКТ, расширение капилляров, застой крови в капиллярах и увеличение проницаемости их стенок, отек окружающих тканей, снижение АД. Рефлекторно возбуждает мозговое вещество надпочечников, способствует выделению эпинефрина, сужению артериол, учащению сердечных сокращений.
Имеются данные о влиянии на секрецию желудочного сока и возможности использования в комплексной терапии язвенной болезни желудка и двенадцатиперстной кишки.
Применение вещества Гистидин
Гепатит, атеросклероз (комплексная терапия).
Противопоказания
Гиперчувствительность, бронхиальная астма, артериальная гипотензия, органические заболевания ЦНС.
Побочные действия вещества Гистидин
Со стороны нервной системы и органов чувств: слабость, головная боль, головокружение, нарушение сознания.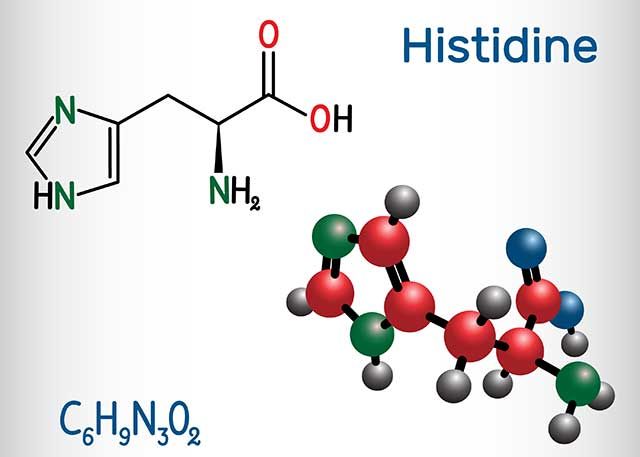
Со стороны органов ЖКТ: диспепсия, тошнота, рвота.
Прочие: снижение АД, бронхоспазм, тремор, парестезия, кожная сыпь, гиперемия кожи, жар, аллергические реакции.
Передозировка
Симптомы: коллапс, отек Квинке, анафилактический шок.
Лечение: назначение антихолинэстеразных средств в сочетании с атропином.
Способ применения и дозы
В/м, по 5 мл 4% раствора ежедневно в течение 25–30 дней, затем по 5–6 инъекций каждые 2–3 мес.
каковы ее свойства, как принимать
Гистидин обычно включают в аминокислотные и витаминные комплексы. Недостаток гистидина может привести к ослаблению слуха и нарушению многих обменных процессов. Гистидин требуется для синтеза большинства белков, а также является предшественником карнозина, обеспечивающего силовую выносливость и препятствующего закислению работающих мышц.
Что представляет из себя гистидин?
Аминокислота гистидин входит в группу протеиногенных – необходимых в синтезе белков, как мышечных, так и например, ферментов.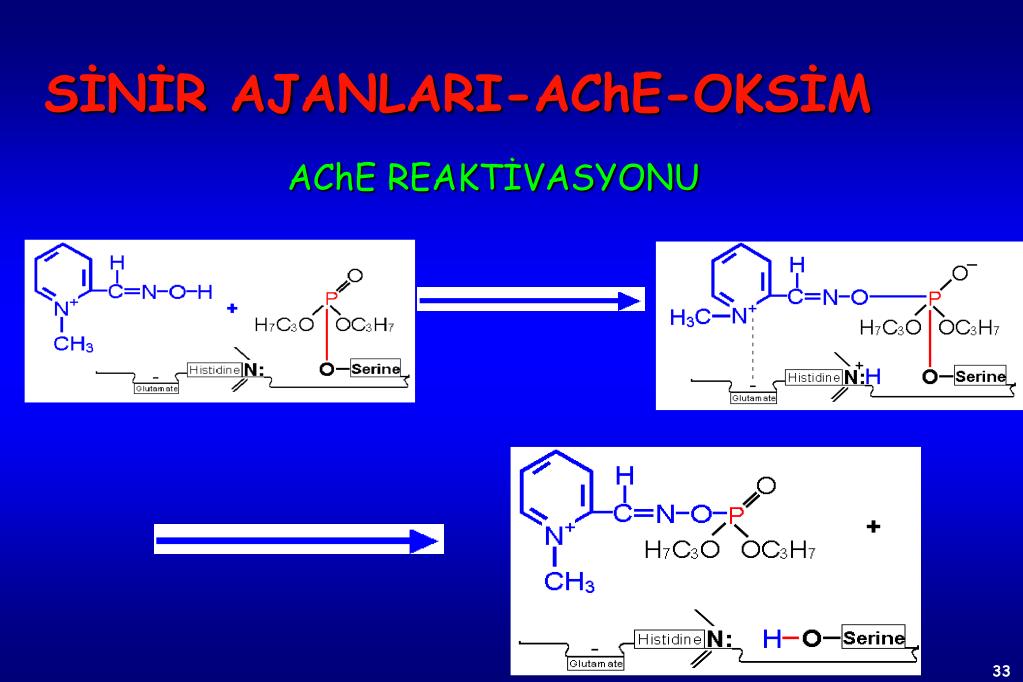 Кроме этого, он выступает предшественником двух важнейших веществ – карнозина и гистамина.
Кроме этого, он выступает предшественником двух важнейших веществ – карнозина и гистамина.
Функции карнозина хорошо известны спортсменам – он выступает мощным антиоксидантом, или буфером молочной кислоты, вырабатывающейся в мышцах под нагрузкой. Чем больше карнозина в мышцах, тем дольше они могут работать до отказа.
Гистамин является важным регулятором множества процессов. Например, хорошо известна его роль в развитии воспалений и аллергических реакций – гистамин вызывает гиперемию, отек тканей, расширение капилляров, спазм гладких мышц, прилив крови к пораженной ткани, выделение адреналина и усиление сердечной и нервной активности. Хотя в некоторых случаях излишне мощная аллергическая или воспалительная реакция организма является опасной и избыточной, в целом гистамин играет важнейшую роль в регенерации и восстановлении тканей.
Формула гистидина
Гистидин относится к классу гетероциклических аминокислот. Формула гистидина содержит в себе т.н. «имидазольное» кольцо – пятичленный цикл, содержащий 2 атома азота. Из-за этого гистидин проявляет больше основные свойства, чем кислотные. Он входит в состав множества ферментов, играя ключевую роль в регуляции всех биохимических процессов организма.
Из-за этого гистидин проявляет больше основные свойства, чем кислотные. Он входит в состав множества ферментов, играя ключевую роль в регуляции всех биохимических процессов организма.
Основные свойства гистидина
Сегодня считается, что гистидин не синтезируется в организме человека (или синтезируется в очень небольших количествах, не покрывающих потребности) и может быть получен только из пищи. Правда, он содержится практически во всех белках, поэтому обычно при нормальном питании его дефицит не возникает.
Важнейшие свойства гистидина состоят в том, что он:
- отвечает за рост и развитие детей,
- регулирует состав крови и ее биохимические параметры, такие как кислотность,
- обеспечивает регенерацию поврежденных тканей,
- участвует в формировании миелиновых оболочек нервов,
- сохраняет работу сердца и сосудов,
- помогает обеспечить нормальный сон,
- ускоряет восстановление после болезней.
Свойства аминокислоты гистидина позволяют сохранять здоровье и нормальное функционирование организма.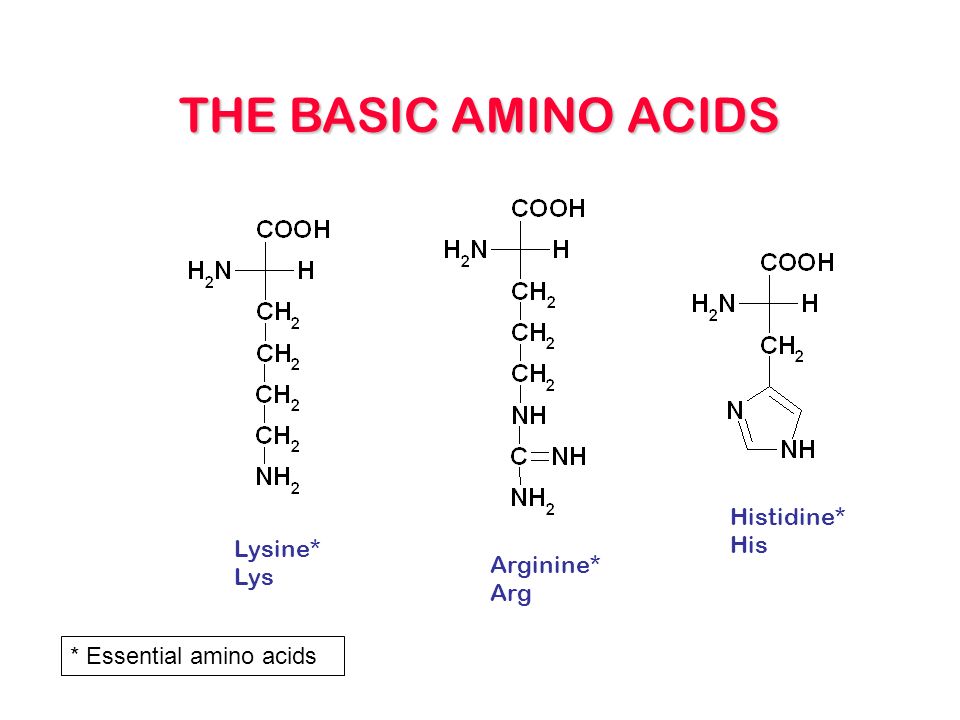 При недостатке этой аминокислоты ухудшается здоровье кожи, развиваются дерматиты, нарушается работа суставов, может возникнуть ревматоидный артрит. Также дефицит гистидина снижает половое влечение, ухудшает работу иммунной системы и вызывает поражение желудка и органов зрения.
При недостатке этой аминокислоты ухудшается здоровье кожи, развиваются дерматиты, нарушается работа суставов, может возникнуть ревматоидный артрит. Также дефицит гистидина снижает половое влечение, ухудшает работу иммунной системы и вызывает поражение желудка и органов зрения.
Какова польза гистидина для организма?
Гистидин настолько важен для организма, что его даже применяют в качестве медицинского препарата, так как он позволяет:
- улучшить секрецию желудочного сока и моторику кишечника,
- стимулирует образование ферментов и повышает эффективность регуляции (защищает от температурных перепадов, скачков давления, влияния радиации и пр.),
- улучшает функцию печени,
- при атеросклерозе улучшает липидный обмен,
- помогает при ревматизме, гепатитах, язве и гастритах, восстанавливает слизистую оболочку желудка,
- улучшает усвоение цинка.
Важно также избегать передозировки гистидина. Хотя у него отсутствуют выраженные побочные эффекты, тем не менее реакция на гистидин организма при переизбытке этой аминокислоты может быть весьма серьезной: слабость, боль в области желудка, тошнота, снижение давления крови, головная боль, нетипичные аллергические реакции.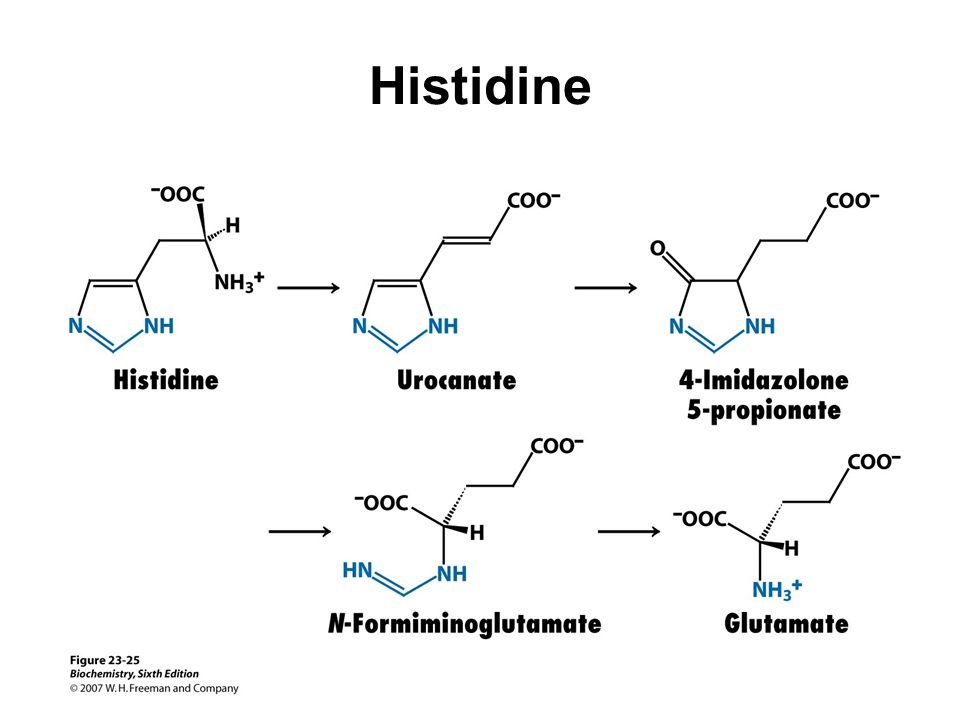 Поэтому прием гистидина необходимо проводить только под контролем врача и в случае реально обнаруженной его нехватки.
Поэтому прием гистидина необходимо проводить только под контролем врача и в случае реально обнаруженной его нехватки.
Какая польза от приема гистидина в спорте?
Спортсменам гистидин может быть интересен как предшественник карнозина и гистамина, проявляющий также адаптогенные свойства. Гистидин способен:
- увеличивать запасы карнозина, повышая работоспособность и выносливость,
- обеспечивать восстановление поврежденных тканей, т.е. ускорять восстановление после тренировок,
- помогать росту мышц (как участвуя в синтезе белка, так и стимулируя выделении соматотропина),
- улучшать состав крови (гистидин входит в состав гемоглобина) и пищеварение,
- повышать устойчивость к изменениям внешней среды (переносить жару и холод, перепады давления и т.п.).
Гистидин проявляет синергические свойства при совмещении с бета-аланином – другим предшественником карнозина, поэтому их совместный прием может еще более улучшить выносливость и ускорить восстановление после тяжелых тренировок или травм.
Улучшение усвоения цинка позволяет сочетать его прием с гистидином, помогая восстанавливать и повышать уровень иммунитета, меньше болеть ОРВИ, а также способствовать выработке тестостерона, улучшая спортивные показатели и либидо.
Как и кому принимать гистидин?
Основным показанием для приема гистидина (за пределами его чисто медицинского применения в терапии различных заболеваний) является его нехватка. Поэтому он хорошо действует при приеме спортсменами во время активных тренировок и соревнований – они постоянно расходуют большое количество ресурсов организма, поэтому им постоянно требуется большое количество витаминов, микроэлементов, белков и аминокислот.
Также гистидин оправдан в ситуациях недостаточного количества белка в пище, во время путешествий и командировок, а также в периоде реабилитации после тяжелых заболеваний и травм.
Чтобы не переусердствовать с гистидином, необходимо следовать рекомендации производителя добавки, а также ориентироваться на суточную норму в 1500-2000 мг в сутки. Или использовать для расчета более точную формулу: 10 мг на каждый килограмм собственного веса в сутки. Спортсмену массой 70 кг при этом потребуется всего 700 мг аминокислоты. В любом случае настоятельно не рекомендуют принимать более 7-8 г гистидина в день, а в случае проблем или вопросов проконсультироваться с врачом.
Или использовать для расчета более точную формулу: 10 мг на каждый килограмм собственного веса в сутки. Спортсмену массой 70 кг при этом потребуется всего 700 мг аминокислоты. В любом случае настоятельно не рекомендуют принимать более 7-8 г гистидина в день, а в случае проблем или вопросов проконсультироваться с врачом.
Гистидин — Энциклопедия Нового Света
Гистидин | |
| Систематическое (ИЮПАК) название | |
| 2-амино-3-(3H-имидазол-4-ил)пропановая кислота | |
| Идентификаторы | |
| CAS-номер | 71-00-1 |
| ПабХим | 773 |
| Химические характеристики | |
| Формула | C 6 H 9 N 3 O 2 |
Мол. масса масса | 155,16 |
| УЛЫБКИ | N[C@@H](Cc1[nH]cnc1)C(O)=O |
| Полные данные | |
Гистидин представляет собой α-аминокислоту, которая часто встречается во многих белках и необходима для питания человека, по крайней мере, для детей. Он является предшественником гистамина и играет важную роль в синтезе пуринов. Подобно аргинину и лизину, гистидин классифицируется как основная аминокислота. Однако боковая цепь гистидина позволяет ему действовать и как основание, и как кислота, как отдавая, так и принимая протоны, что может иметь большое значение в его роли в составе белков.
L-изомер гистидина, который является единственной формой, участвующей в синтезе белка, является одной из 20 стандартных аминокислот, распространенных в животных белках и необходимых для нормального функционирования человека. Гистидин по-разному классифицируется как «условно незаменимая» или «незаменимая» аминокислота. Незаменимая аминокислота — это такая аминокислота, которая не может быть синтезирована человеческим организмом из других соединений посредством химических реакций или со скоростью, достаточной для удовлетворения физиологических потребностей организма, и поэтому должна поступать с пищей. Младенцы не могут эффективно синтезировать гистидин, что делает его необходимым для питания младенцев. Исторически он считался несущественным для взрослых, которые могут какое-то время обходиться без него в рационе, но сегодня он обычно считается необходимым и для взрослых.
Незаменимая аминокислота — это такая аминокислота, которая не может быть синтезирована человеческим организмом из других соединений посредством химических реакций или со скоростью, достаточной для удовлетворения физиологических потребностей организма, и поэтому должна поступать с пищей. Младенцы не могут эффективно синтезировать гистидин, что делает его необходимым для питания младенцев. Исторически он считался несущественным для взрослых, которые могут какое-то время обходиться без него в рационе, но сегодня он обычно считается необходимым и для взрослых.
Сложная координация на молекулярном уровне проявляется в роли гистидина и других аминокислот. Способность белка функционировать зависит от координации ряда аминокислот, объединенных вместе и работающих в гармонии. Некоторые аминокислоты играют важную роль в свертывании белка, который должен принять точную конформационную форму, чтобы функционировать. Уникальная боковая цепь гистидина придает белкам, содержащим гистидин, также уникальные свойства.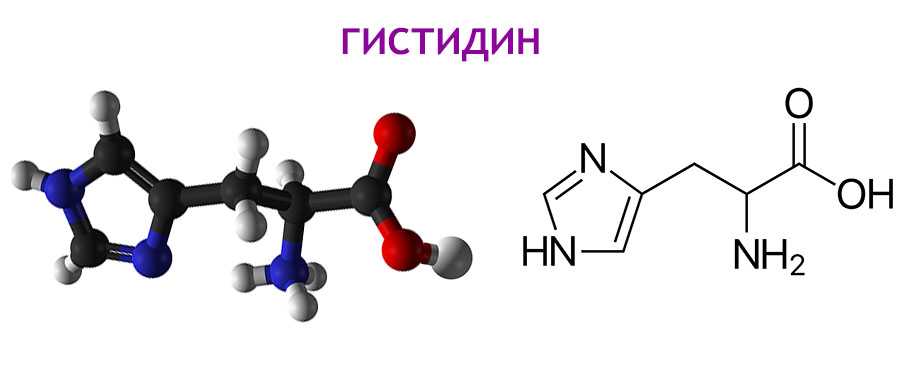 Затем белок выполняет особую роль, например, фермента, катализирующего химические реакции. Если аминокислоты комбинируются неправильно, эта сложная координация нарушается.
Затем белок выполняет особую роль, например, фермента, катализирующего химические реакции. Если аминокислоты комбинируются неправильно, эта сложная координация нарушается.
Содержимое
- 1 Структура
- 2 Химические свойства
- 3 источника
- 4 Дополнительные изображения
- 5 Каталожные номера
- 6 Внешние ссылки
- 7 кредитов
Незаменимые аминокислоты, такие как гистидин, показывают важность личной ответственности и дисциплины при выборе диеты для получения всех элементов, необходимых для хорошего здоровья.
Трехбуквенный код гистидина — His, его однобуквенный код — H, а его систематическое название — 2-амино-3-(1H-имидазол-4-ил)-
пропановая кислота (IUPAC-IUB 1983).
Структура
В биохимии термин «аминокислота» часто используется для обозначения альфа-аминокислот : тех аминокислот, в которых амино- и карбоксилатные группы присоединены к одному и тому же углероду, так называемому α-углероду ( альфа-углерод).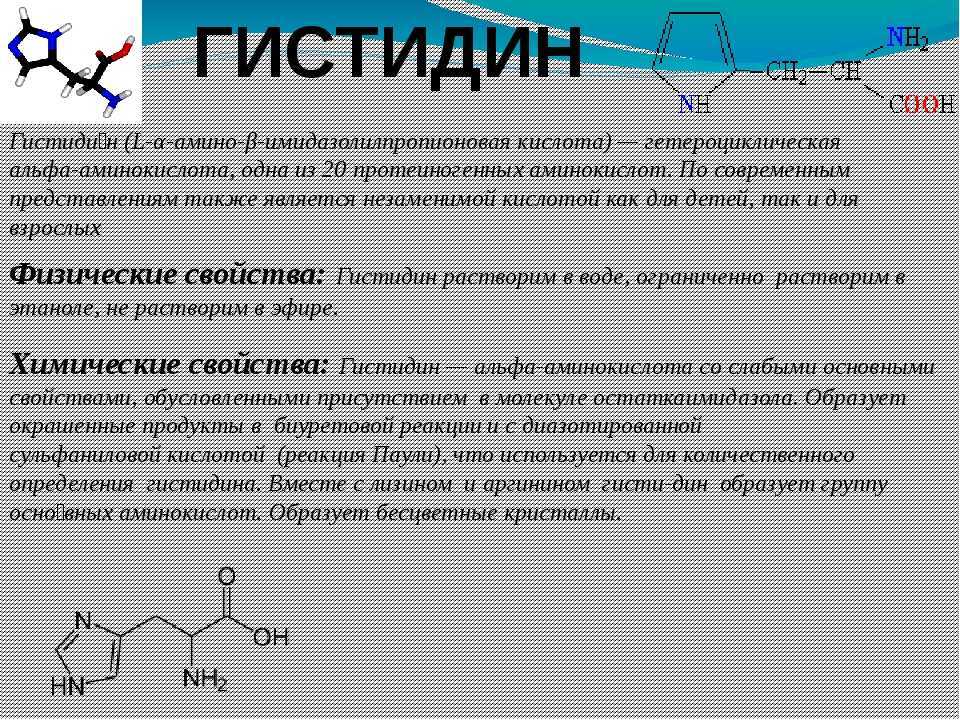 Общая структура этих альфа-аминокислот:
Общая структура этих альфа-аминокислот:
Р | H 2 N-C-COOH | ЧАС
, где R представляет собой боковую цепь , специфичную для каждой аминокислоты. Исключением из этой базовой структуры является пролин, боковая цепь которого зацикливается на основной цепи, образуя кольцевую структуру, в которой вторичная аминогруппа заменяет первичную аминогруппу.
Связанная с гистидином гемовая группа сукцинатдегидрогеназы, переносчика электронов в митохондриальной цепи переноса электронов. Большая полупрозрачная сфера указывает на местонахождение ирониона.
Большинство аминокислот встречаются в виде двух возможных оптических изомеров, называемых D и L. Аминокислоты L представляют подавляющее большинство аминокислот, содержащихся в белках. Их называют протеиногенными аминокислотами. Как следует из названия «протеиногенные» (буквально, строящие белок), эти аминокислоты кодируются стандартным генетическим кодом и участвуют в процессе синтеза белка.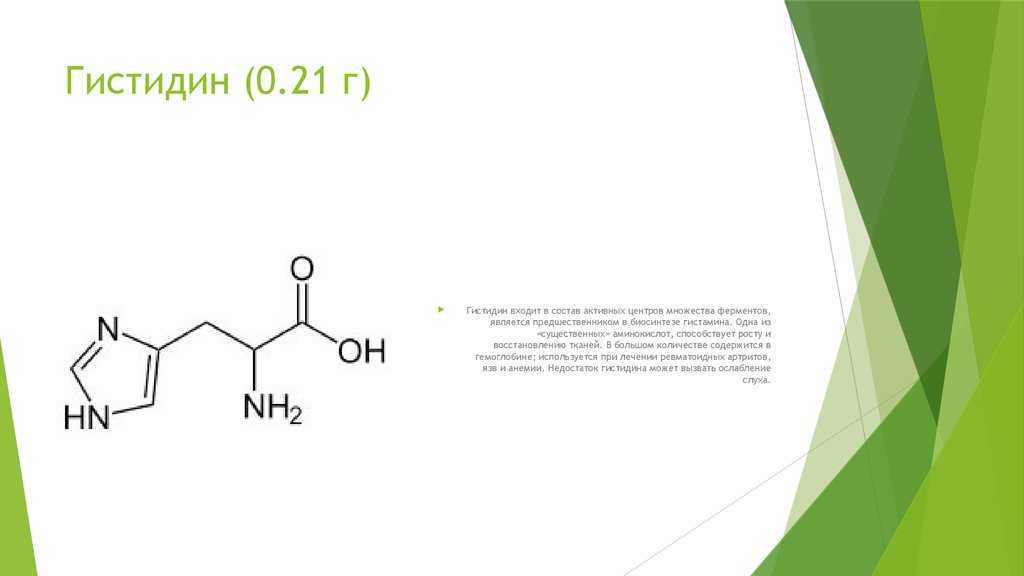 Существует два энантиомера гистидина, D-гистидин и L-гистидин, но только L-стереоизомер участвует в синтезе белков млекопитающих.
Существует два энантиомера гистидина, D-гистидин и L-гистидин, но только L-стереоизомер участвует в синтезе белков млекопитающих.
Общая химическая формула гистидина: C 6 H 9 N 3 O 2 (IUPAC-IUB 1983).
Химическая структура имидазола
Гистидин имеет имидазольную боковую цепь. Имидазол представляет собой гетероциклическое ароматическое органическое соединение. (Гетероциклические соединения представляют собой органические соединения, которые содержат кольцевую структуру, содержащую атомы в дополнение к углероду, такие как сера, кислород или азот, как часть кольца.) Имидазол относится к исходному соединению C 3 H 4 N 2 , тогда как имидазолы представляют собой класс гетероциклов с похожей кольцевой структурой, но разными заместителями. Эта кольцевая система присутствует в гистидине и родственном ему гормоне гистамине. Имидазол может действовать как основание и как слабая кислота.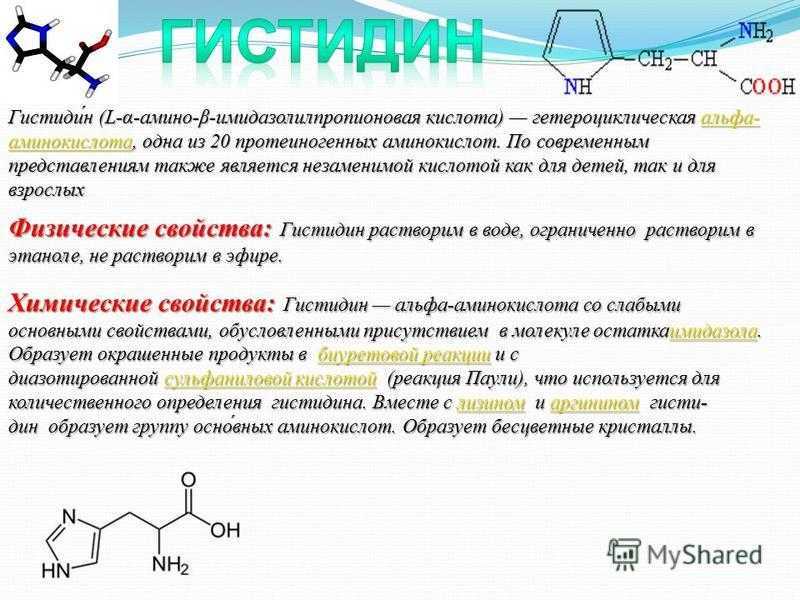 Имидазол существует в двух таутомерных формах, в которых атом водорода перемещается между двумя атомами азота.
Имидазол существует в двух таутомерных формах, в которых атом водорода перемещается между двумя атомами азота.
Даже в слабокислых условиях происходит протонирование азота, изменяющее свойства гистидина и полипептида в целом. Он используется во многих белках в качестве регуляторного механизма, изменяя конформацию и поведение полипептида в кислых областях, таких как поздняя эндосома или лизосома, вызывая изменение конформации ферментов.
Химические свойства
Имидазольные боковые цепи и относительно нейтральная pKa гистидина (около 6,0) означают, что относительно небольшие сдвиги клеточного pH будут изменять его заряд. По этой причине боковая цепь этой аминокислоты находит широкое применение в качестве координирующего лиганда в металлопротеинах, а также в качестве каталитического центра в некоторых ферментах, таких как поддержка каталитических функций химотрипсина (пищеварительного фермента) и тех ферментов, которые участвуют в метаболизме. белков и углеводов.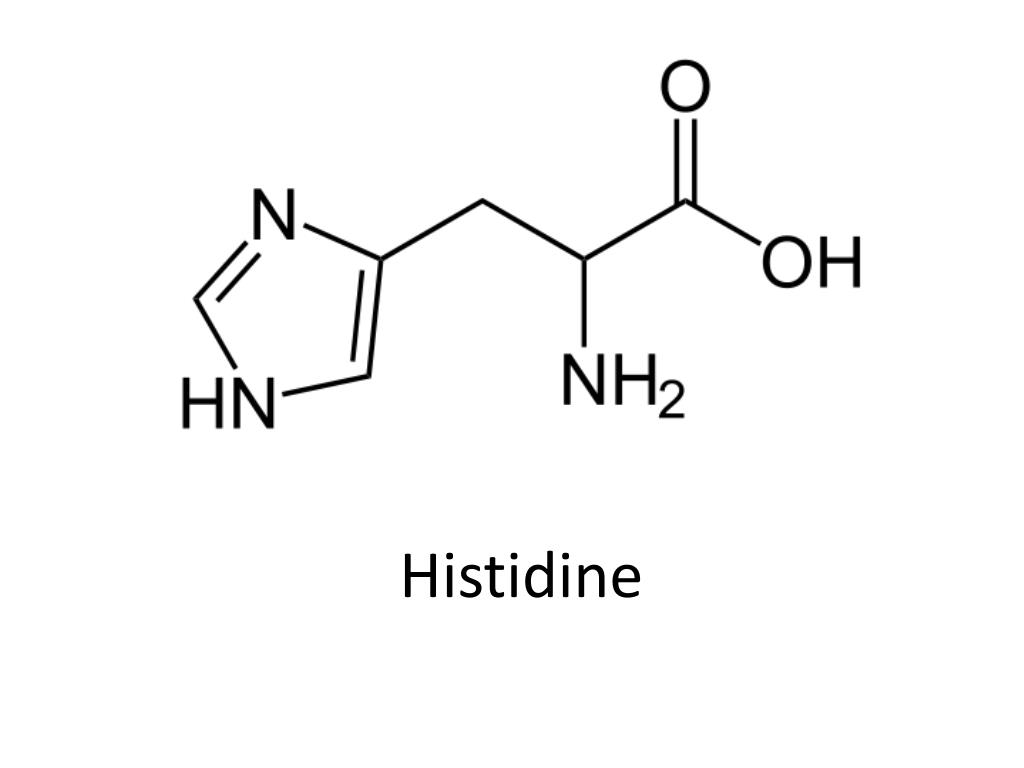
По сути, боковая цепь имидазола имеет два атома азота с разными свойствами: один связан с водородом и отдает свою неподеленную пару ароматическому кольцу и поэтому является слегка кислым, тогда как другой отдает только одну электронную пару кольцу, поэтому он имеет свободную одинокую пару и является основным. То есть из-за своей уникальной боковой цепи гистидин может действовать и как кислота, и как основание, как отдавая, так и принимая протоны. Эти свойства по-разному используются в белках. В каталитических триадах (три аминокислотных компонента, находящихся внутри активного центра некоторых протеазных ферментов: серин, аспартат и гистидин) основной азот гистидина используется для отрыва протона от серина, треонина или цистеина, чтобы активировать его как нуклеофил. . В гистидиновом челноке протонов гистидин используется для быстрого перемещения протонов; он может сделать это, отделив протон от его основного азота, чтобы получить положительно заряженный промежуточный продукт, а затем использовать другую молекулу, буфер, для извлечения протона из его кислого азота.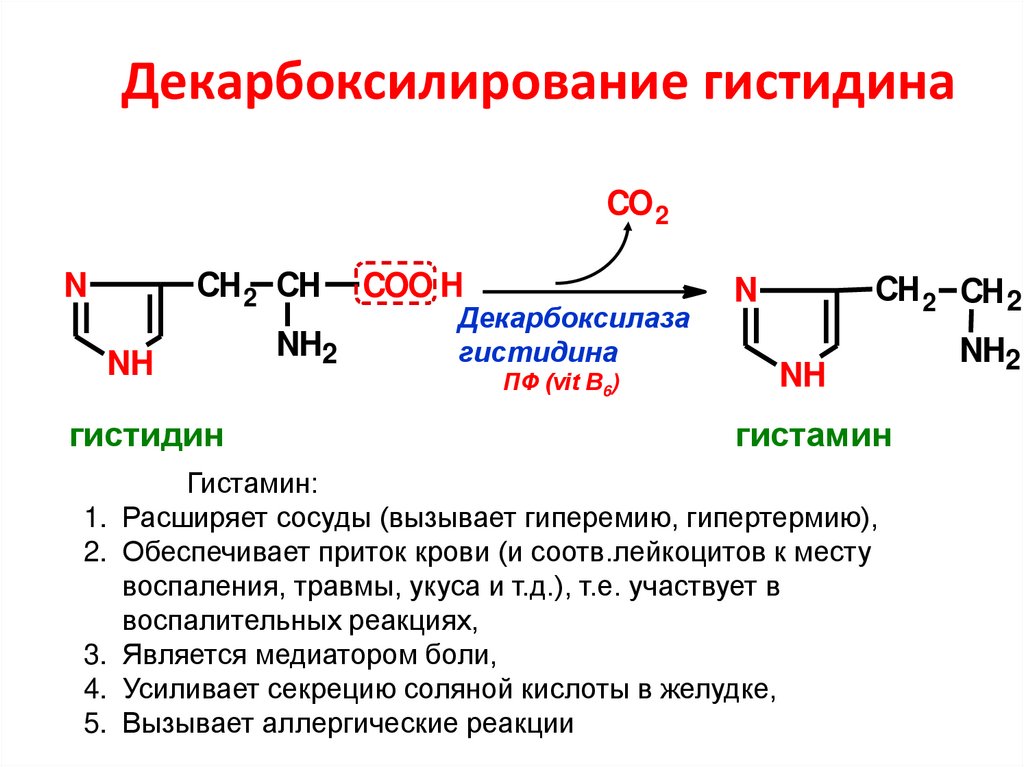 В карбоангидразах гистидиновый протонный челнок используется для быстрого перемещения протонов от молекулы воды, связанной цинком, для быстрой регенерации активной формы фермента.
В карбоангидразах гистидиновый протонный челнок используется для быстрого перемещения протонов от молекулы воды, связанной цинком, для быстрой регенерации активной формы фермента.
Гистидин является предшественником биосинтеза гистамина и карнозина.
Превращение гистидина в гистамин под действием гистидиндекарбоксилазы
Фермент гистидинаммиак-лиаза превращает гистидин в аммиак и урокановую кислоту. Дефицит этого фермента наблюдается при редком нарушении обмена веществ гистидинемии.
Источники
Гистидин содержится во фруктах, таких как бананы и виноград, мясе и птице, молоке и молочных продуктах. Он также содержится в корнеплодах и всех зеленых овощах, хотя и в меньших количествах.
Дополнительные изображения
Гистидин
Ссылки
Ссылки ISBN поддерживают NWE за счет реферальных сборов. В GD Fasman, ed., Прогнозирование белковых структур и принципы белковой конформации .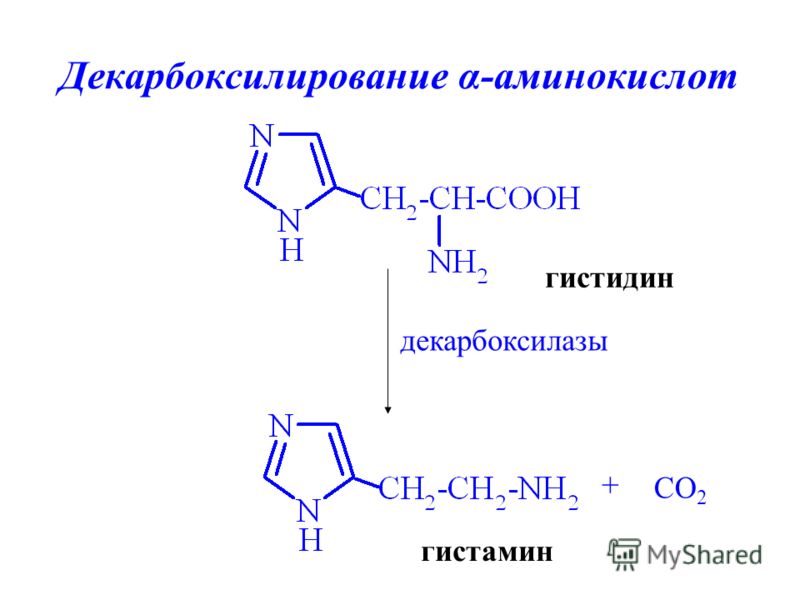 Нью-Йорк: Пленум Пресс, 1989. ISBN 0306431319
Нью-Йорк: Пленум Пресс, 1989. ISBN 0306431319
Внешние ссылки
Все ссылки получены 9 января 2018 г.
- Биосинтез гистидина (ранние стадии)
- Биосинтез гистидина (поздние стадии)
- Катаболизм гистидина
| Основные семейства биохимических веществ | ||
| Пептиды | Аминокислоты | Нуклеиновые кислоты | Углеводы | Нуклеотидные сахара | липиды | Терпены | каротиноиды | Тетрапирролы | Кофакторы ферментов | Стероиды | Флавоноиды | Алкалоиды | Поликетиды | Гликозиды | ||
| Аналоги нуклеиновых кислот: | 20 общих аминокислот | Аналоги нуклеиновых кислот: |
Авторы
New World Encyclopedia авторы и редакторы переписали и дополнили статью Википедии
в соответствии со стандартами New World Encyclopedia .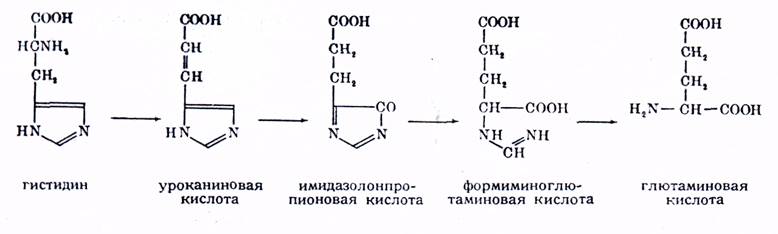 Эта статья соответствует условиям лицензии Creative Commons CC-by-sa 3.0 (CC-by-sa), которая может использоваться и распространяться с надлежащим указанием авторства. Упоминание должно быть выполнено в соответствии с условиями этой лицензии, которая может ссылаться как на авторов New World Encyclopedia , так и на самоотверженных добровольных участников Фонда Викимедиа. Чтобы процитировать эту статью, щелкните здесь, чтобы просмотреть список допустимых форматов цитирования. История более ранних вкладов википедистов доступна исследователям здесь:
Эта статья соответствует условиям лицензии Creative Commons CC-by-sa 3.0 (CC-by-sa), которая может использоваться и распространяться с надлежащим указанием авторства. Упоминание должно быть выполнено в соответствии с условиями этой лицензии, которая может ссылаться как на авторов New World Encyclopedia , так и на самоотверженных добровольных участников Фонда Викимедиа. Чтобы процитировать эту статью, щелкните здесь, чтобы просмотреть список допустимых форматов цитирования. История более ранних вкладов википедистов доступна исследователям здесь:
- Гистидин история
- Имидазол история
История этой статьи с момента ее импорта в New World Encyclopedia :
- История «Histidine»
Примечание. На использование отдельных изображений, лицензированных отдельно, могут распространяться некоторые ограничения.
FSANZ одобряет изменение уровня L-гистидина в детских смесях Nestlé
Nestlé Australia Limited и Nestlé New Zealand Limited подали заявку в мае 2012 года, добиваясь снижения минимального требования к L-гистидину во всех продуктах для детского питания.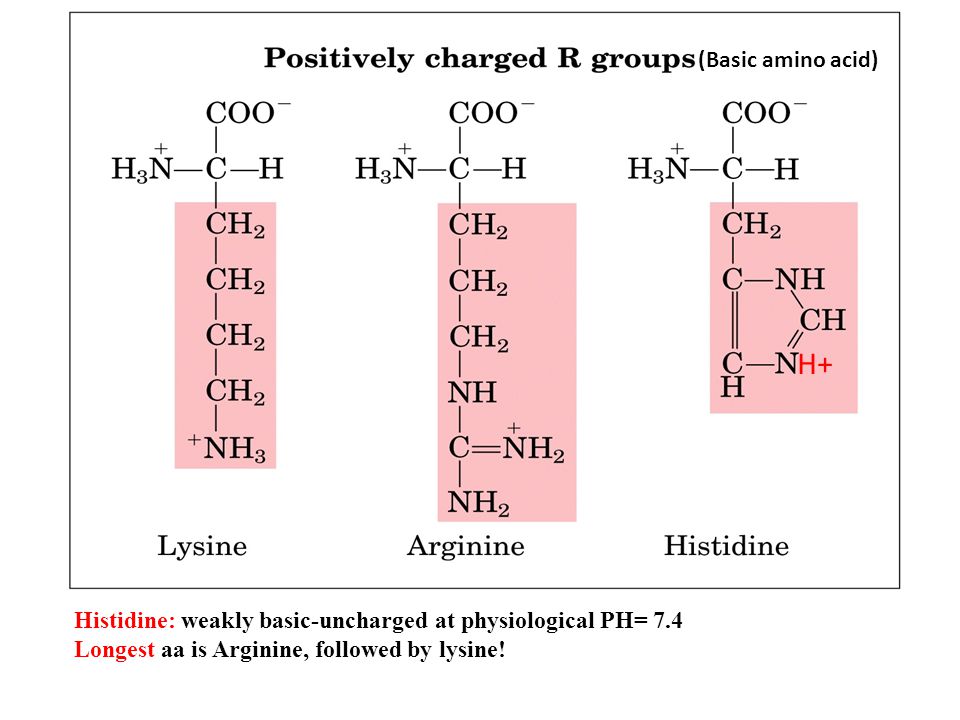
Они предложили внести поправку в Кодекс пищевых стандартов Австралии и Новой Зеландии, уменьшив минимальные требования с 12 мг/100 кДж до 10 мг/100 кДж.
L-гистидин, естественным образом присутствующий в грудном молоке, является химическим предшественником гистамина, помогает поддерживать здоровье сердца и системы кровообращения, а также укрепляет иммунную систему.
В своем заявлении Nestlé утверждала, что предлагаемое сокращение «безопасно и будет способствовать нормальному росту и развитию младенцев». Он добавил, что поправка будет способствовать согласованности международного регулирования, что будет полезно для торговли.
«Соответствующее» снижение
«На основании нашей оценки FSANZ считает целесообразным снизить минимально необходимый уровень L-гистидина в детских смесях с 12 мг/100 кДж до 10 мг/100 кДж в соответствии с запросом заявителя. », — говорится в проекте поправки FSANZ .
«Сниженный минимальный уровень сравним со средним содержанием L-гистидина в грудном молоке и считается достаточным для поддержки роста детей, находящихся на искусственном вскармливании».
«Внесение поправок в Кодекс обеспечит соответствие между Кодексом и международными и зарубежными стандартами на пищевые продукты и в целом принесет чистую пользу сообществу», – говорится в уведомлении .
Сравнительная оценка пищевой безопасности (CNSA) была проведена для проверки заявки Nestlé.
С помощью оценки FSANZ стремился подтвердить, будет ли предлагаемое снижение соответствовать уровням L-гистидина в грудном молоке и поддерживать нормальный рост детей, находящихся на искусственном вскармливании.
CNSA установила, что средний уровень L-гистидина в грудном молоке составляет 24 мг L-гистидина на грамм сырого протеина, что эквивалентно 10 мг/100 кДж.
Гармонизация нормативно-правовой базы
По данным Nestlé, действующие правила FSANZ не соответствуют соответствующим международным стандартам.
Стандарт Кодекса для детских смесей и смесей для специальных медицинских целей, предназначенных для младенцев, устанавливает минимальную потребность L-гистидина в детской смеси 41 мг/100 ккал – примерно 10 мг/100 кДж.
