Аминокислоты картинки: ⬇ Скачать картинки D0 b0 d0 bc d0 b8 d0 bd d0 be d0 ba d0 b8 d1 81 d0 bb d0 be d1 82 d1 8b, стоковые фото D0 b0 d0 bc d0 b8 d0 bd d0 be d0 ba d0 b8 d1 81 d0 bb d0 be d1 82 d1 8b в хорошем качестве
%d0%b0%d0%bc%d0%b8%d0%bd%d0%be%d0%ba%d0%b8%d1%81%d0%bb%d0%be%d1%82%d1%8b PNG, векторы, PSD и пнг для бесплатной загрузки
естественный цвет bb крем цвета
1200*1200
схема бд электронный компонент технологии принципиальная схема технологическая линия
2000*2000
green environmental protection pattern garbage can be recycled green clean
2000*2000
ма дурга лицо индуистский праздник карта
5000*5000
дизайн плаката премьера фильма кино с белым вектором экрана ба
1200*1200
набор векторных иконок реалистичные погоды изолированных на прозрачной ба
800*800
be careful to slip fall warning sign carefully
2500*2775
blue series frame color can be changed text box streamer
1024*1369
3d модель надувной подушки bb cream
2500*2500
вектор поп арт иллюстрацией черная женщина шопинг
800*800
в первоначальном письме bd логотипа
1200*1200
дизайн логотипа bc значок буквы b
8333*8333
розовый бб крем красивый бб крем ручная роспись бб крем мультфильм бб крем
2000*3000
be careful with fire pay attention to fire pay attention to fire warning icon
2000*2000
крем крем вв вв на воздушной подушке иллюстрация
2000*2000
Золотая буква b логотип bc письмо дизайн вектор с золотыми цветами
8334*8334
три группы 3d реалистичное декоративное яйцо с золотым цветом на гнезде bd с золотым всплеском текстовый баннер
5000*5000
буква bc 3d логотип круг
1200*1200
Воздушная подушка cc крем косметика косметика по уходу за кожей плакат пресная Воздушная подушка bb крем cc
3240*4320
logo design can be used for beauty cosmetics logo fashion
1024*1369
bd письмо 3d круг логотип
1200*1200
облака комиксов
5042*5042
в первоначальном письме bd шаблон векторный дизайн логотипа
1200*1200
логотип bc
1200*1200
в первоначальном письме ба логотипа
1200*1200
элегантный серебряный золотой bb позже логотип значок символа
1200*1200
bb крем cc крем пудра Порошок торт фонд
2000*2000
в первоначальном письме векторный дизайн логотипа шаблон
1200*1200
chinese wind distant mountain pine tree chinese style pine tree chinese style poster can be combined
3600*2475
prohibited use mobile phone illustration can not be used
2048*2048
сложный современный дизайн логотипа с биткойн символами и буквами bc
8331*8331
Красивая розовая и безупречная воздушная подушка bb крем косметика постер розовый красивый розовый Нет времени На воздушной
3240*4320
Креативное письмо bb дизайн логотипа черно белый вектор минималистский
1202*1202
be careful of road slip warning signs fall warning signs character warning signs pattern warning signs
2000*2000
в первоначальном письме bd логотип шаблон
1200*1200
в первоначальном письме bd шаблон векторный дизайн логотипа
1200*1200
номер 82 золотой шрифт
1200*1200
bb крем ню макияж косметика косметика
1200*1500
круглая буквица bd или db дизайн логотипа вектор
5000*5000
логотип готов использовать год до н э
6667*6667
bc beauty косметический логотип дизайн вектор
8542*8542
Векторная иллюстрация мультфильм различных овощей на деревянном ба
800*800
black key that can be hung on the body car key key
2000*2000
аэрозольный баллончик увлажняющий лосьон bb cream парфюм для рук
3072*4107
flowering in spring flower buds flowers to be placed plumeria
2000*2000
bb логотип письмо дизайн вектор простые и минималистские ключевые слова lan
1202*1202
be careful and fragile warning signs round beware
2500*2000
bb логотип дизайн шаблона
2223*2223
bb логотип градиент с абстрактной формой
1200*1200
испуганные глаза комиксов
5042*5042
Пищевые аминокислоты — Компания НЕО Кемикал
Аминокислоты — основной элемент построениях всех белков. Они делятся на заменимые, незаменимые и условно незаменимые.
Они делятся на заменимые, незаменимые и условно незаменимые.
Незаменимые аминокислоты – те аминокислоты, которые не могут быть синтезированы в организме человека и должны поступать в организм с пищей.
Условно незаменимыми кислотами называются аминокислоты, которые синтезируются организмом человека при определенных условиях. Часто организм испытывает недостаток этих аминокислот.
К заменимым относятся аминокислоты, которые наш организм способен синтезировать самостоятельно.
ВСАА — это комплекс из трех незаменимых аминокислот: L-лейцин, L-изолейцин и L-валин, основной материал для построения новых мышц. Составляют 35% всех аминокислот в мышцах и принимают важное участие в процессах анаболизма и восстановления, обладают антикатаболическим действием. BCAA не могут синтезироваться в организме, поэтому получать человек их может только с пищей и специальными добавками. BCAA в первую очередь метаболируются в мышцах, их можно рассматривать как основное «топливо» для мышц, которое повышает спортивные показатели, улучшает состояние здоровья, к тому же они абсолютно безопасны.
L — Валин — Один из главных компонентов в росте и синтезе тканей тела. Вместе с лейцином и изолейцином служит источником энергии в мышечных клетках, а также препятствует снижению уровня серотонина. Также необходим для поддержания нормального обмена азота в организме, входит в состав практически всех известных белков, является незаменимой аминокислотой не синтезируется в организме человека и поэтому должен поступать с пищей. Входит в состав ВСАА.
L — Лейцин — Лейцин входит в состав природных белков, применяется для лечения болезней печени, анемий и других заболеваний. В среднем суточная потребность организма в лейцине для здорового человека составляет 4-6 грамм. Входит в состав ВСАА и многих БАД
L — Изолейцин — это аминокислота входящая в состав всех природных белков. Является незаменимой аминокислотой, что означает, что изолейцин не может синтезироваться в организме человека и должен поступать в него с пищей. Участвует в энергетическом обмене..
Участвует в энергетическом обмене..
L — Глутамин – одна из 20 стандартных аминокислот, входящих в состав белка. Самая распространенная аминокислота организма, мышцы состоят из неё на 60%. Широко используется в спортивном питании и при производстве БАД.
Креатин – Креатин чаще всего используется для повышения эффективности физических нагрузок и увеличения мышечной массы у спортсменов. Существуют научные исследования, поддерживающие использование креатина для улучшения спортивной активности молодых и здоровых людей во время кратковременной интенсивной активности и нагрузки
Фото аминокислоты. Картинки аминокислоты перуанский женьшеня, Стоковые Фотографии и Роялти-Фри Изображения аминокислоты перуанский женьшеня
Картинки аминокислоты перуанский женьшеня, Стоковые Фотографии и Роялти-Фри Изображения аминокислоты перуанский женьшеня
bigacim.gmail.com
3110 x 2037
bigacim.gmail.com
4176 x 2992
bigacim.gmail.com
3849 x 3190
bigacim.gmail.com
4404 x 3384
bigacim.gmail.com
3279 x 2153
bigacim.gmail.com
2999 x 2994
bigacim.gmail.com
4187 x 2824
sablinstanislav
2291 x 3055
sablinstanislav
2291 x 3055
sablinstanislav
2291 x 3055
sablinstanislav
3240 x 2160
sablinstanislav
3240 x 2160
sablinstanislav
2291 x 3055
sablinstanislav
3240 x 2160
sablinstanislav
3055 x 2291
sablinstanislav
3240 x 2160
sablinstanislav
3240 x 2160
sablinstanislav
3240 x 2160
sablinstanislav
2291 x 3055
ru.depositphotos.com
Картинки аминокислоты bcaa, Стоковые Фотографии и Роялти-Фри Изображения аминокислоты bcaa
Syda_Productions
4901 x 3267
Syda_Productions
4245 x 2830
Syda_Productions
3042 x 1977
Syda_Productions
4245 x 2830
Syda_Productions
4245 x 2830
Syda_Productions
3467 x 2311
Syda_Productions
4245 x 2830
Syda_Productions
4245 x 2830
Syda_Productions
4245 x 2830
Syda_Productions
3478 x 2304
ru. depositphotos.com
depositphotos.com
виды, свойства и фото :: SYL.ru
Химические соединения, которые выступают в роли составляющих веществ белков, это и есть аминокислоты. В аптеке они могут быть представлены в разных видах: в форме порошка, капсул, таблеток или раствора.
Общее описание
Выделяют среди таких элементов около 20 протеиногенных веществ.
Классифицируют их на три класса:
- заменимый;
- условно заменимый;
- незаменимый.
Внимание! Все виды запускаются в единую цепочку процессов анаболического характера для поддержания положительного баланса азота, который находится в мышцах. За счет этого подавляется и предотвращается разрушительный процесс. Если отсутствует одно соединение, может произойти целая череда плохих последствий. Это могут быть как нарушения работы ЖКТ, так и ослабление иммунной системы в целом. Поэтому организму спортсмена важно получать необходимое количество добавок. Они способствуют нормализации хода обменных процессов. Приобрести аминокислоты в аптеке сегодня не вызывает сложностей.
Заменимые
Вещества синтезируются в человеческом организме из других составляющих.
Выделяют следующие аминокислоты:
- аспарагиновая кислота;
- глютаминовая;
- пролин;
- аланин;
- аспарагин;
- серин.
Незаменимые
Эта категория представляет кислоты, которые не синтезируются в организме. Их поступление с пищей необходимо организму.
Незаменимым считают попадание в организм следующих веществ:
- валина; находится в мясных, молочных, зерновых продуктах, также в арахисе и сое;
- гистидина; содержится в тунце, свиной вырезке, говядине, куриной грудке, лососе, соевых бобах, чечевице и арахисе;
- изолейцина; представлен в составе миндаля, кешью, курином мясе, яйце, рыбе, горохе турецком, печени, чечевице, сое, ржи, семенах различных типов;
- лейцина; в таких продуктах как бурый рис, орехи, семена, мясо, рыба, чечевица;
- лизина; в рыбных, мясных, молочных продуктах, орехах и пшенице;
- метионина; в мясных, молочных и рыбных изделиях, яйцах и бобовых;
- треонина; содержится в составе молочных продуктов, яйцах, также в бобах и орехе;
- триптофана; его можно обнаружить в молочке, мясе, овсе, банане, кунжуте, арахисе, кедре, также в рыбном, курином и индюшином мясе;
- фенилаланина; в твороге, молоке, курице, рыбных изделиях, бобовых, говядине.

Условно незаменимые
Чаще подлежат синтезу непосредственно организмом. Однако в стрессовых ситуациях в форме физических нагрузок или заболевания возможна их выработка в недостающем количестве. Бывают случаи отсутствия синтеза вовсе. Такие аминокислоты в аптеке также можно купить.
Основные аминокислоты:
- Глютамин. Помимо молочных и мясных продуктов можно наблюдать их в свекле, шпинате, капусте, петрушке.
- Аргинин. Подразумевает медикаментозные препараты, пищевые добавки для спортсменов или для стимуляции иммунитета.
- Тирозин. Достаточное количество поступает в организм с белками в пище, дефицит их в основном не обнаруживается.
- Цистеин. Находится в большинстве белков, из которых образуется гидролиз; сырье для получения кератинов – волосы, перья, рога и прочее.
- Глицин. Зарегистрирован в виде пищевых добавок под кодом Е640 для модификации аромата и вкусовых качеств, содержится в медикаментозных препаратах.
Описание комплекса для роста мышц
Совокупность элементов из белка представляет собой комплекс аминокислот. В аптеке их чаще приобретают бодибилдеры, ведь мышцы почти целиком состоят из белков. Они необходимы для того, чтобы мышечные волокна, росли, укреплялись и восстанавливались.
Внимание! Стоит отметить и свойства комплекса, которые способствуют выработке гормонов.
От данных элементов увеличиваются сила и выносливость, восстанавливается психическое состояние по окончанию тренировок, происходит расщепление подкожных жиров и улучшается рабочий процесс головного мозга. Можно купить аминокислоты в аптеке, название, однако, может быть неизвестным для покупателя. Специалист проконсультирует по данному вопросу и поможет подобрать подходящий препарат.
Распространенные комплексы
Сегодня можно купить следующие аминокислоты в аптеке для роста мышц:
- L-глютамин. Является самым распространенным веществом для организма человека. Выпускается в таблетках и капсулах.

- Гистидин. Представлен в форме капсул, раствор которых водят внутримышечно.
- Аминокислоты и аминокислотные комплексы. Можно увидеть на прилавках магазинов спортивного питания.
Важно! Не рекомендуют совершать покупки данного вещества в интернет-магазинах, потому что вероятен риск подделок.
- BCAA – уложенные в стеклянной таре капсулы или таблетки на выбор.
- Таурин — выпускают в форме таблеток, порошка и капсул. Может содержаться в составе таких препаратов, как «Пептамен», «Дибикор» и прочие.
- L-аргинин (вазотон). Кроме капсул и таблеток можно приобрести в форме биологически активных добавок и других витаминов.
Лейцин, валин, изолейцин считаются самыми оказывающими действие на развитие, поддержание в тонусе и восстановление мышечной массы. Прием этих препаратов одновременно способствуют максимальному воздействию их на организм. Такого рода аминокислоты в аптеке приобретают по доступной цене в нужном количестве.
www.syl.ru
Что такое аминокислоты и для чего они нужны? :: SYL.ru
Большинство людей знает, что в организме человека есть аминокислоты. Они поддерживают наше здоровье и играют важную роль в функционировании организма в целом. Но что такое аминокислоты и какие именно являются жизненно необходимыми? Попробуем разобраться в этом вопросе подробнее.
Что такое аминокислоты?
Если говорить простыми словами, то подобные вещества представляют собой строительный материал, необходимый для синтеза тканевых белков, пептидных гормонов и других физиологических соединений. То есть аминокислоты и белки – вещи очень тесно связанные, так как именно без аминокислот образование белков невозможно. Кроме того, они выполняют и другие функции:
- Участвуют в работе головного мозга. Они могут играть роль нейромедиаторов – химических веществ, которые передают импульс с одной клетки на другую.
- Способствуют нормальной работе витаминов и минералов.
- Снабжают энергией ткани мышц.

Их функции
Самая основная функция – образование белков. Аминокислоты создают элемент, без которого нормальная жизнедеятельность невозможна. Эти вещества содержатся в продуктах (творог, мясо, яйца, рыба), но также присутствуют и в добавках. В зависимости от последовательности аминокислот белки могут иметь разные биологические свойства. Ведь они являются регуляторами процессов, протекающих в клетках.
Они также поддерживают азотистое равновесия – от этого также зависит нормальное функционирование человеческого организма. Отметим, что не все аминокислоты содержатся в продуктах или создаются нашим организмом. Есть и такие, которые можно получить только извне – их называют незаменимыми.
Основные группы
Всего в природе ученые смогли обнаружить 28 аминокислот (из них 19 заменимых и 9 незаменимых). Большинство растений и бактерий способны самостоятельно создавать нужные им вещества из существующих неорганических соединений. В теле человека также синтезируется большинство нужных аминокислот – их называют заменимыми. К ним относятся:
- Аргинин, апанин, глицин, серин, цистеин, таурин, аспарагин, глутамин, аспаригиновая кислота, тирозин, цитруллин, орнитин.
- Существуют также частично заменимые аминокислоты – гистидин и аргинин.
Все эти элементы могут использоваться организмом для производства белка. Как мы уже знаем, существуют и незаменимые аминокислоты. Они не могут создаваться организмом человека. Однако они также необходимы для его нормального функционирования. К ним относятся: изолейцин, метионин, лизин, валин, треонин, фенилаланин, триптофан, лейцин.
Они поступают в человеческий организм с пищей. Отметим, что процесс создания белков в организме идет постоянно. И если хотя бы одна незаменимая аминокислота отсутствует, то синтез на время приостанавливается. В результате недостатка белка рост организма приостанавливается. В результате этого масса тела падает, а обмен веществ нарушается. При острой недостаточности аминокислот организм может и погибнуть.
Незаменимые
Мы уже знаем, какие аминокислоты относятся к этой категории. Рассмотрим их подробнее:
- Валин – это один из самых важных компонентов, который восстанавливает разрушенные мышечные ткани организма и поддерживает обмен азота в теле. Благодаря ему уровень серотонина поддерживается на нормальном уровне. При этом мышечная координация повышается. Это основной компонент для построения новых мышц, и без него функционирование организма невозможно. Молекулы аминокислот находятся в таких продуктах, как куриное филе, яйца, говядина, грецкие орехи, лосось.
- Гистидин – еще один важный компонент, который также восстанавливает мышечные ткани. В отличие от валина, он присутствует в миелиновых оболочках, защищающих нервные клетки. Какие функции выполняет? Это вещество также защищает организм от действия радиации и выводит из него тяжелые металлы. Из гистидина синтезируется мышечный антиоксидант – карнозин. Для пополнения запаса этой аминокислоты рекомендуют употреблять в пищу тунца, чечевицу, арахис, куриное филе.
- Изолейцин – пожалуй, один из самых важных элементов. Он принимает участие в создании гемоглобина, а также благодаря ему у человека поддерживается нормальный уровень сахара в крови. Эта аминокислота укрепляет наружный слой кожи, нормализует процессы энергообеспечения и принимает участие в построении новых мышц. Содержится в сыре, курином филе, рыбе, индейке, яйцах.
- Лейцин – аминокислота, принимающая ключевое участие в укреплении и поддержке иммунной системы. Это вещество нормализует метаболические процессы, усиливает синтез белка, а также препятствует разрушению белковых молекул и распаду глюкозы, нормализует водный обмен и повышает секрецию инсулина в организме. Входит аминокислота в состав BCAA (материал для создания новых мышечных тканей). Она содержится в твороге, курином филе, говядине, то есть мясных и молочных продуктах.
- Лизин – материал для создания костных тканей, который также принимает участие в усвоении кальция.
 Это его основная роль. Но также лизин участвует в синтезе гормонов, антител, восстановлении тканей. Он хорошо влияет на работу сердца, усиливает сопротивляемость организма вирусам и снижает уровень триглицеридов, содержащихся в крови. Источниками этой аминокислоты является мясо птицы и говядины, а также горох и фасоль.
Это его основная роль. Но также лизин участвует в синтезе гормонов, антител, восстановлении тканей. Он хорошо влияет на работу сердца, усиливает сопротивляемость организма вирусам и снижает уровень триглицеридов, содержащихся в крови. Источниками этой аминокислоты является мясо птицы и говядины, а также горох и фасоль. - Метионин – незаменимая аминокислота, участвующая в жировом обмене и влияющая на синтез других аминокислот – цистеина и таурина. Кроме этого ей приписывают следующие положительные эффекты: улучшение выносливости мышц, понижение уровня плохого холестерина, улучшение эффективности переработки пищи, улучшение работы печени, отвод тяжелых металлов из организма и защита от радиации. Как и ранее, лучшими источниками этого элемента является мясо курицы и индейки, телятина. Но также он присутствует в твороге, арахисе, бобовых культурах.
- Треонин – элемент для поддержки белкового метаболизма. Он принимает участие в образовании эластина и коллагена, не позволяет жирам откладываться в печени и оказывает хорошее воздействия на сердечно-сосудистую и нервную систему. Треонин содержится в уже знакомых нам продуктах: мясе, рыбе, молочных продуктах, орехах, бобовых.
- Триптофан – важная аминокислота, основная задача которой – создание серотонина. Подобный элемент называют «источником радости», он поднимает настроение и подавляет депрессию, может излечить человека от бессонницы. Также его присутствие в организме облегчает ПМС у женщин. Содержится в мясе, рыбе, сырах, бобовых, молочных продуктах.
- Фенилаланин – элемент, который улучшает память человека, снижает болевые ощущения и улучшает настроение, подавляет аппетит. Находится эта аминокислота в молекулах белков, которые составляют сухожилья, мышцы и связки. Лучшими источниками фенилаланина являются яйца, мяса, орехи, фасоль и другие бобовые культуры.
- Аланин – участвует в метаболизме, а также повышает сокращение мышц и является источником энергии для нервной системы. Благодаря аланину уровень сахара в крови стабилизируется, иммунная система работает лучше.
 Хорошими источниками этой аминокислоты является любое мясо, сыр и молоко.
Хорошими источниками этой аминокислоты является любое мясо, сыр и молоко.
Заменимые аминокислоты
Какие аминокислоты относятся к заменимым?
- Аргинин – обладает большим количеством положительных свойств, что делает этот элемент востребованным и ценным. Его положительные свойства: препятствует росту злокачественных образований, нормализует азотный баланс, улучшает эффективность процесса дезинтоксикации печени, способствует выработке сперматозоидов и инсулина, улучшает кровоток в мышечных тканях, повышает иммунитет. Источники: куриные яйца, свинина, семечки тыквы, грецкие и другие орехи.
- Аспарагин – способствует улучшению работы нервной системы, повышает иммунитет благодаря повышению антител и иммуноглобулинов. Среди продуктов лучшими источниками являются морепродукты, птица, бобовые, молоко.
- Цитруллин – важная для мышц и организма в целом аминокислота, укрепляющая иммунную систему, повышающая энергообеспечение. Она усиливает выносливость, улучшает эректильную функцию. Содержится в основном в арбузах, бобовых, арахисе.
- Цистеин – принимает участие в формировании тканей волос и кожи. Также формирует и поддерживает структуру пептидов и белков. Содержится в овсе, мясе, рыбе.
- Диметилглицин – входит в состав нейромедиаторов, определенных гормонов и ДНК. Содержится в мясе, бобовых, зернах, печени.
- Глютамин – позволяет нормально работать мышечным тканям, укрепляет иммунную систему, участвует в синтезе белка мышц, ускоряет процессы восстановления, нормализует уровень сахара и даже улучшает работу головного мозга. Содержится в мясе курицы, рыбе, молоке, капусте, петрушке.
- Глутатион – антиоксидант, положительно влияющий на жировой обмен и защищающий организм от токсинов, вирусов, болезней. Содержится в луке, чесноке, орехах, семечках, сельдерее, яичных желтках.
- Глицин – благодаря ему возможен синтез желчных и нуклеиновых кислот и заменимых аминокислот. Кроме этой основной функции есть и второстепенные: улучшение качества сна, восстановление поврежденных тканей, улучшение работы ЦНС, противовоспалительные действия.
 Набор продуктов, в которых содержится эта аминокислота, стандартен: молоко, мясо, яйца, рыба.
Набор продуктов, в которых содержится эта аминокислота, стандартен: молоко, мясо, яйца, рыба. - Аминомасляная кислота (гамма) – важный элемент, являющийся нейромедиатором головного мозга и ЦНС. Обладает полезными свойствами, благодаря которым пользуется популярностью среди бодибилдеров: вырабатывает гормоны роста, улучшает процесс сжигания жиров, улучшает качество сна. Содержится в кофе, чае, грибах.
- Глутаминовая кислота – нейромедиатор, передающий импульсы в нервную систему. Хорошо влияет на углеводный обмен, является источником энергии для головного мозга. Содержится в любом мясе, горошке, молочных продуктах.
- Густамин – является нейротрансмиттером нервной системы, повышает половое влечение и проницаемость кровеносных сосудов.
- Орнитин – также способствует выработке гормонов роста, улучшает процесс сжигания жиров и хорошо влияет на печень. Из-за этого часто употребляется бодибилдерами. Содержится в мясе, яйцах, рыбе, молочных продуктах.
- Пролин – укрепляет суставы, связки, сердечно-сосудистую систему.
- Серин – улучшает работу иммунной системы, влияет на жировой обмен.
- Таурин – способствует нормализации натрия, магния, калия, хорошо влияет на головной мозг и обменные процессы организма.
- Тирозин – способствует выработке мелатонина, влияет на щитовидную железу, подавляет аппетит. Считается, что тирозин является творческой аминокислотой, поскольку позволяет думать масштабнее и открывает в человеке творческие способности. Содержится в миндале, бананах, семечках, кунжуте, авокадо.
- Карнитин – также относится к аминокислотам из-за схожей химической структуры. С его помощью жирные кислоты эффективно перерабатываются в энергию, он хорошо влияет на работу сердца и печени, повышает выносливость, замедляет старение, понижает уровень холестерина. Его большое содержание замечено в баранине, молочных продуктах, свинине, телятине, индейке.
Содержание в продуктах
Как вы уже поняли, есть основные категории продуктов, где содержится большое количество аминокислот: мясо (чаще всего мясо птиц), яйца, молочные продукты, бобовые и зелень.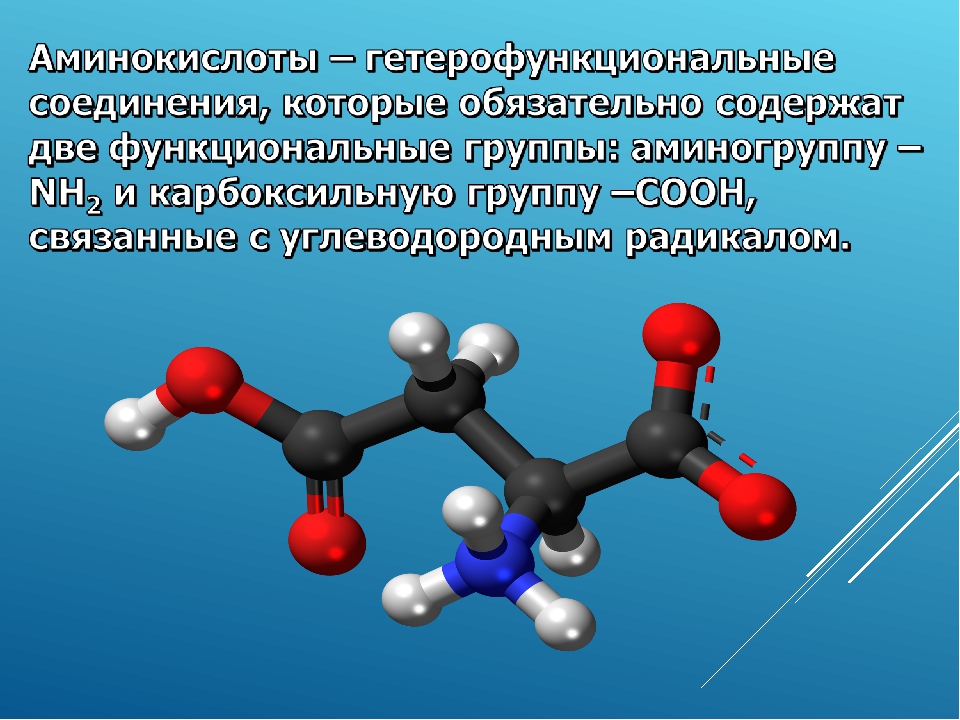 Однако почти в любых продуктах есть небольшое содержание тех или иных элементов. Поэтому крайне важно разнообразить свой рацион.
Однако почти в любых продуктах есть небольшое содержание тех или иных элементов. Поэтому крайне важно разнообразить свой рацион.
Применение аминокислот в медицине
Учитывая, что такое аминокислоты и какова их роль, очень важно, чтобы в организме их было в достаточном количестве. Людям, которые страдают недостатком этих элементов, назначают специальные диеты и препараты, содержащие в себе конкретные аминокислоты. Помните о том, что прием медицинских препаратов возможен только с назначением врача:
- Лейцин содержится в различных БАДах, препаратах для лечения печени и анемии. Он также используется как усилитель вкуса Е641.
- Фенилалинин применяется для лечения болезни Паркинсона, используется в производстве жевательной резинки и напитков с газами.
- Лизин – средство обогащения продуктов питания и кормов животных.
- Триптофан назначается при чувстве страха, депрессии, сильных физических нагрузках.
- Изолейцин используется для лечения неврозов, его назначают при стрессах, слабости. Также многие антибиотики содержат в своем составе этот элемент.
- Гистидин всегда есть в составе препаратов для лечения язв, артритов. Также он содержится во всевозможных витаминных комплексах.
Назначение
Специальные добавки, содержащие большое количество аминокислот, могут назначать мужчинам и женщинам, которые часто подвергаются физическим нагрузкам. Спортсмены, занимающиеся бодибилдингом, спринтом, разным единоборствам и фитнесом, чаще всего употребляют специальные добавки на основе аминокислот. Но также и людям с разными заболеваниям назначают либо специальные диеты, либо препараты с содержанием необходимых аминокислот.
Необходимость
Теперь вы знаете, что такое аминокислоты, и понимаете их основные функции. Мы назвали все известные на данный момент элементы, которые принимают участие в синтезе белков. Можно сказать, что все белки состоят из аминокислот разного типа. Они необходимы для нормального функционирования организма.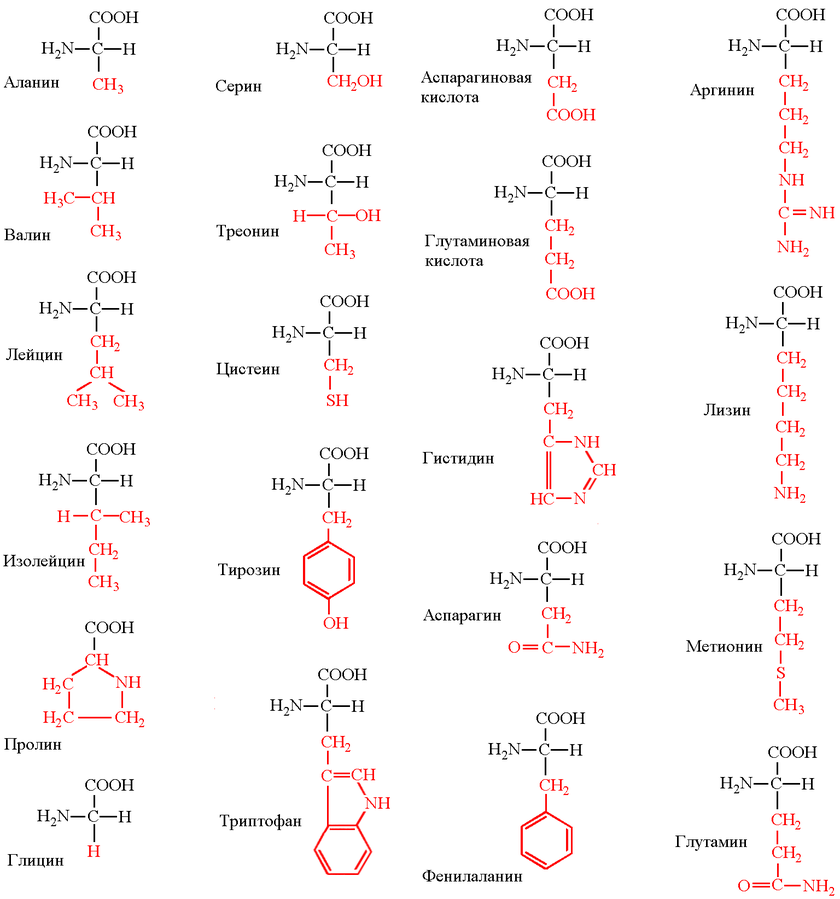
Цистин
Действующее вещество – цистин. Выпускается в форме таблеток и капсул.
Препарат способен замедлять процесс старения в организме, используется как антиоксидант, эффективен при артритах. Показания: бронхиальная астма, анемия, болезнь Альцгеймера, заболевания дыхательной системы, цистит, алкоголизм, дефицит белка, инфекционные заболевания, также используется для улучшения зрения.
Дозировка и длительность лечения определяется лечащим врачом в зависимости от диагноза и состояния пациента.
Побочные действия: аллергические реакции, дискомфорт в области ЖКТ.
Противопоказания: индивидуальная непереносимость компонентов, беременность, период лактации, цистинурия.
Если Вам понравилась наша статья и Вам есть что добавить, поделитесь своими мыслями. Нам очень важно знать Ваше мнение!
woman-l.ru
Картинки amino, Стоковые Фотографии и Роялти-Фри Изображения amino
Syda_Productions
4901 x 3267
Leonid_Andronov
9282 x 4062
Syda_Productions
3042 x 1977
Leonid_Andronov
9732 x 6083
bigacim.gmail.com
3110 x 2037
matka_Wariatka
3744 x 5616
matka_Wariatka
3744 x 5616
Leonid_Andronov
10000 x 5721
Leonid_Andronov
9439 x 6195
Leonid_Andronov
7027 x 3557
ru.depositphotos.com
Аминокислоты. Свойства аминокислот. Аминокислоты в организме человека
Бытует мнение, что человеческое тело на 70-80% состоит из воды. С этим сложно поспорить, однако помимо жидкости есть еще один вид веществ, являющийся базовым компонентом живого организма. Речь идет о белках. Последние, в свою очередь, образованы аминокислотами. Вот им-то, а также их значению для здоровья и посвящена данная статья.
Фото: аминокислоты
Что такое аминокислоты
Как вы уже поняли, аминокислоты представляют собой микроскопические «кирпичики», из которых состоят протеины — главный строительный материал организма человека. Эти соединения имеют органическое происхождение. Их отличительной чертой является присутствие в молекулярной структуре сразу аминных и карбоксильных групп.
Эти соединения имеют органическое происхождение. Их отличительной чертой является присутствие в молекулярной структуре сразу аминных и карбоксильных групп.
Об аминокислотах научному миру стало известно в не таком уж далеком прошлом — всего-то в начале XIX-го столетия. Первое соединение данного ряда было открыто ученым А. Браконно, и стал им глицин. Указанное вещество исследователь выделил из желатина в 1820 году. О последней из известных на сегодняшний день аминокислоте человечество узнало спустя 105 лет: в 1925 году С. Шрайвер получил из рыбного белка гидроксилизин.
Физические свойства протеиновых компонентов не имеют ничего общего с таковыми оснований и кислот. Составляющие белков — это кристаллические вещества. Большинство из них имеют сладкий вкус и плавятся при довольно-таки внушительных температурах. Все без исключения вещества данного типа растворяются как в органических растворителях, так и в обычной воде, однако в последней делают это гораздо лучше. Подводя итог, можно смело заявить о том, что компонентам белка присущ солеобразный характер.
Виды аминокислот
Все составляющие протеинов классифицируют на две группы: незаменимые и заменимые.
Незаменимые аминокислоты названы так потому, что человеческое тело не имеет возможности самостоятельно синтезировать эти соединения для собственных нужд. То есть он должен получать такие вещества извне — с продуктами питания и соответствующими биодобавками. К категории незаменимых аминокислот относятся: валин, метионин, лейцин, изолейцин, лизин, триптофан, треонин, фенилаланин.
Что собой представляют заменимые белковые составляющие? Это органические вещества, без проблем вырабатываемые человеческим организмом. В данную группу входят следующие соединения: аланин, серин, глицин, аспарагиновая кислота.
Есть еще третья категория белковых составляющих — условно-незаменимые. Организм человека умеет их синтезировать, однако производит в минимальных количествах. Из-за этого развивается дефицит органических соединений во внутренней среде тела, а это приводит к негативным последствиям для здоровья. К условно-незаменимым аминокислотам принадлежат гистидин, аргинин, тирозин, глютамин, пролин, цистеин.
К условно-незаменимым аминокислотам принадлежат гистидин, аргинин, тирозин, глютамин, пролин, цистеин.
Аминокислоты в организме человека
20% человеческого тела приходится на протеины. Это говорит о том, что можно даже не сомневаться в необходимости аминокислот человеку для нормальной жизнедеятельности его организма.
Основополагающей функцией данных органических соединений является построение клеточной структуры. Второе по важности полезное свойство аминокислот — транспортировка питательных компонентов. Однако этими двумя пунктами деятельность белковых составляющих в организме человека вовсе не ограничивается. Аминокислоты необходимы для производства белков, обеспечения упругости и эластичности кожи, красоты волос. Они участвуют в производстве ферментов, обеспечивают хорошее настроение, не допускают наступление стресса и нервных расстройств, устраняют бессонницу и повышают качество сна. Без аминокислот невозможны здоровье костей, заживление повреждений телесных покровов, отличная память и умение концентрироваться на объектах и выполняемых действиях.
Большое значение имеют составляющие белка для спортсменов, особенно тех, кто занимается физической культурой на профессиональном уровне. Дело в том, что одной из функций аминокислот является восстановление мышечной ткани после тренировки. А еще эти органические вещества помогают увеличить объем мускулатуры.
Фото: аминокислоты
Аминокислоты благотворно влияют на метаболизм, улучшая и ускоряя его. Они принимают участие в образовании гормонов, поддерживают тело человека в тонусе, борются со свободными радикалами, не допускают возникновение и дальнейшее развитие раковых клеток, нормализуют работу практически всех жизненноважных органов. Составляющие белков замедляют процессы старения и способны продлить жизнь.
Это был обзор общих функций аминокислот. Но у каждого протеинового кирпичика имеется также свой арсенал полезных для здоровья человека свойств. Давайте кратко познакомимся с ними.
Свойства незаменимых аминокислот
- Фенилаланин — спазмолитик, облегчает депрессивный синдром.
- Валин, изолейцин, лейцин — аминокислоты ВСАА, защищающие мышечные волокна от разрушений при занятиях спортом и стимулирующие рост мышц.
- Треонин — нужен для образования эластина и коллагена, для укрепления зубов, костей, сердца, связок.
- Триптофан — действует как болеутоляющее, ему свойственен успокоительный и снотворный эффект.
- Метионин — работает как жиросжигатель, снабжает организм человека серой, предотвращает развитие болезней сердца.
- Лизин — нужен для производства гормона роста, ускоряет заживление слизистых оболочек, сравнительно быстро восстанавливает мышцы.
Свойства заменимых аминокислот
- Аланин — дает мышцам энергию, участвует в обмене углеводов, снижает уровень сахара в крови, активизирует иммунитет.
- Серин — улучшает обмен жиров и повышает иммунитет.
- Глицин — благодаря данному веществу синтезируются желчные и нуклеиновые кислоты. Он оказывает благотворное воздействие на функцию мозга и психологическое состояние.
- Аспарагиновая кислота — требуется для усвоения организмом минеральных солей.
Свойства условно-незаменимых аминокислот
- Аргинин — принимает участие в возникновении оксида азота, способствует расширению кровеносных сосудов, активизирует работу иммунной системы, понижает содержание в крови холестерина.
- Гистидин — мощный антиоксидант.
- Глутамин — иммуномодулятор, отличный восстановитель поврежденных мышц.
- Тирозин — повышает работоспособность, выносливость, препятствует возникновению явления перетренированности у спортсменов.
- Цистеин — требуется для поддержания упругости кожи, для нормализации веса за счет сжигания жиров, обеспечивает рост мышц.
- Пролин — делает кожу более плотной, без него невозможен процесс заживления ран.

Фото: аминокислоты
Недостаток той или иной аминокислоты негативно сказывается на здоровье человека. Дефицит составляющих белка чреват возникновением проблем со сном, раздражительностью, ломкостью ногтей, выпадением волос. Вероятны и более серьезные последствия: гипертония, сахарный диабет, ожирение, артрит, остеопороз. От нехватки аминокислот страдают как молодые, так и пожилые люди. Чтобы ее избежать, необходимо сбалансировать рацион и принимать специальные биодобавки.
Автор: Пономаренко Надежда Статья защищена законом об авторских и смежных правах. При использовании и перепечатке материала активная ссылка на женский сайт www.inmoment.ru обязательна!
Теги: аминокислоты, свойства аминокислот, аминокислоты в организме человека
Вернуться в начало раздела Фитнес и спортВернуться в начало раздела Красота и Здоровье
www.inmoment.ru
Аминокислоты в поляризованном свете • Олег Соколенко • Научная картинка дня на «Элементах» • Физика, Биология
Это не абстрактная живопись, а фотография кристаллов двух аминокислот — L-глутамина и бета-аланина (см. β-Alanine). Снимок попал в Топ-20 престижного международного конкурса микрофотографии Nikon Small World 2020.
Автор снимка, американский фотограф Джастин Цолль, присылает на конкурс свои фотографии аминокислот уже три года, а на его персональном сайте таких снимков еще больше. Каждый из них изумительно красив и не похож на другие цветом, формой или настроением — хотя это каждый раз всё те же две аминокислоты! Цолль не ученый, для него эти микрофотографии — искусство, а также источник средств к существованию: он продает постеры со своими произведениями. Для своих работ фотограф перепробовал практически все доступные субстанции, включая соль и сахар. Кроме смеси L-глутамина и бета-аланина его фаворитом какое-то время был ментол (см. фото 1, фото 2 и фото 3).
Чтобы сотворить такие шедевры, Джастин сначала растворяет аминокислоты в воде с этиловым спиртом высокой степени очистки (фактически, в водке).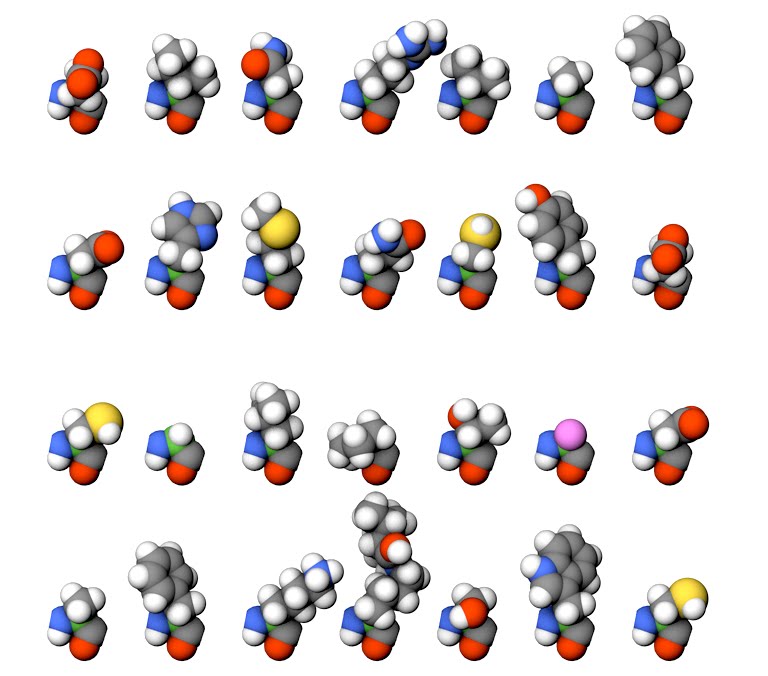 Получившуюся смесь он наносит на предметные стекла, которые затем высушивает, нагревая. Каждый раз приходится отсмотреть множество препаратов, чтобы выбрать среди них фотогеничный. Когда препарат выбран, фотограф делает несколько десятков снимков разных его участков, из которых потом собирает панораму — для максимальной детализации. Снимки делаются с 40-кратным увеличением, которое дает окуляр микроскопа Olympus Bh3 и объектив фотокамеры.
Получившуюся смесь он наносит на предметные стекла, которые затем высушивает, нагревая. Каждый раз приходится отсмотреть множество препаратов, чтобы выбрать среди них фотогеничный. Когда препарат выбран, фотограф делает несколько десятков снимков разных его участков, из которых потом собирает панораму — для максимальной детализации. Снимки делаются с 40-кратным увеличением, которое дает окуляр микроскопа Olympus Bh3 и объектив фотокамеры.
Цветовая палитра снимков — результат использования поляризационных фильтров. Один из фильтров ставится перед источником света, второй — перед линзой фотоаппарата. Кристаллы аминокислот оптически анизотропны, скорость световых лучей, идущих по разным направлениям внутри кристалла, различна, что приводит к двойному лучепреломлению (см. картинку дня Двойное лучепреломление). Поэтому при такой двойной поляризации света возникает яркая и разнообразная интерференционная окраска (подробнее о том, как это происходит, см. в картинке дня Оливин в поляризованном свете). Сами по себе кристаллы как L-глутамина, так и бета-аланина бесцветны.
Осталось сказать несколько слов про сами аминокислоты. L-глутамин — встречающаяся в природе (в отличие от ее зеркального D-изомера) форма глутамина. Эта аминокислота не является незаменимой, то есть синтезируется в нашем организме в достаточном количестве; она участвует во множестве процессов, включая синтез углеводов и нуклеиновых кислот, работу иммунной системы и передачу нервных сигналов. Бета-аланин тоже синтезируется в нашем организме и является предшественником карнозина — естественного антиоксиданта, повышающего выносливость мышц. Кроме мышц его много также в тканях головного мозга.
Фото © Justin Zoll с сайта nikonsmallworld.com. Увеличение 40×.
Олег Соколенко
Для чего нужны аминокислоты и как их принимать?
Аминокислоты – одни из самых популярных добавок в ассортименте спортивного питания. Их используют для быстрого роста, укрепления и восстановления мышечной ткани после интенсивных тренировок. Дополнительный прием таких нутриентов особенно нужен бодибилдерам, пауэрлифтерам, тяжелоатлетам, а также тем, кто ведет здоровый, активный образ жизни.
Дополнительный прием таких нутриентов особенно нужен бодибилдерам, пауэрлифтерам, тяжелоатлетам, а также тем, кто ведет здоровый, активный образ жизни.
Аминокислоты: виды и предназначение
По своей сути аминокислоты являются белками, расщепленными на частицы. Когда белок распадается (например, в процессе пищеварения), он образовывает эти питательные вещества. Таким образом, аминокислотные комплексы практически не требуют времени для усвоения организмом, и быстрее проникают в мышечные клетки, питая и восстанавливая их.
Все аминокислоты можно разделить на три вида:
- заменимые (которые могут вырабатываться в организме человека) – это аланин, аспаргин, глицин, пролин, глютамин, серин;
- условно заменимые (вырабатываются только в благоприятных условиях или только у взрослых людей) – аргинин, цистеин, тирозин;
- все остальные аминокислоты относятся к категории незаменимых (они не вырабатываются самостоятельно и поступают в организм только с продуктами рациона).
В организме эти нутриенты выполняют множество функций:
- отвечают за создание новых клеток, а также регенерацию мышечных волокон;
- обеспечивают организм дополнительной энергией;
- способствуют нормальному обмену веществ, поддержанию здорового гормонального фона;
- улучшают память, повышают концентрацию внимания, влияют на состояние нервной системы;
- поддерживают иммунную систему;
- подавляют аппетит и способствуют избавлению от лишнего веса;
- играют важную роль при формировании мышечного рельефа;
- улучшают состояние волос, ногтей и кожи.
Если вы занимаетесь спортом, отдельное внимание следует обратить на комплекс ВСАА. Он состоит из трех незаменимых аминокислот – лейцина, изолейцина и валина, препятствующих распаду мышечных волокон (катаболизму). Принимайте этот вид спортпита, чтобы защитить мышцы во время интенсивной тренировки или сразу после нее.
Аминокислоты одинаково важны и для мужчин, и для женщин.![]() Но если представители сильного пола используют их для прироста мышечной массы, то женщины таким образом избавляются от избытков жировой ткани.
Но если представители сильного пола используют их для прироста мышечной массы, то женщины таким образом избавляются от избытков жировой ткани.
Как употреблять аминокислоты?
Прежде всего, любое спортивное питание лучше выбирать в надежном, специализированном магазине. Здесь представлена сертифицированная продукция, прошедшая многочисленные исследования и официально допущенная к продаже. Чего не скажешь о сомнительном содержимом ярких баночек, выставленных на рыночных прилавках или торговых точках.
С целью набрать мышечную массу аминокислоты принимают с утра и после каждой тренировки, для похудения – несколько чаще. Рекомендуемая однократная доза составляет от 5 до 20 грамм. Соблюдайте инструкцию и не превышайте дозировку – таким образом вы не усилите эффект от спортивной добавки, но создадите лишнюю нагрузку на печень и почки.
Аминокислотные комплексы хорошо сочетаются с другими видами спортивного питания. Но, если вы дополнительно принимаете гейнер или протеин, проконсультируйтесь со своим тренером. Сегодня на рынке представлены аминокислоты в различных формах – капсулах, таблетках, порошках. Все они равнозначны по эффективности, потому вы легко подберете наиболее удобный для себя вариант.
ТОП-7 рейтинг аминокислот, представленных в нашем магазине BCAA.UA
На нашем сайте представлены только лучшие аминокислоты, но благодаря вашим отзывам, мы сумели определить 7 топовых товаров, которые можно купить у нас в магазине:
1). BCAA 700 мг 200 капсул
2). BCAA Zero 360 грамм
3). BCAA Xline 300 грамм
4). Bcaa Xplode 500 грамм
5). Xtend 1260 грамм
6). Amino 5600 500 таблеток
7). Amino X 1,01 кг
Эксперты составили перечень портящих зрение продуктов — Российская газета
Первое место в нем занимает — приготовленный из пшеничной муки высшего сорта белый хлеб. В нем много рафинированного крахмала, который заставляет поджелудочную железу вырабатывать больше инсулина. А он в больших количествах негативно влияет на глазное яблоко и способствует развитию близорукости. Большое количество кофе и алкоголя сужает сосуды и нарушает кровообращение глаз. Кроме того, спиртное также воздействует на определенные участки коры головного мозга, влияющих на зрительное восприятие человека.
Большое количество кофе и алкоголя сужает сосуды и нарушает кровообращение глаз. Кроме того, спиртное также воздействует на определенные участки коры головного мозга, влияющих на зрительное восприятие человека.
«Мусорная еда» — разнообразные бургеры, газировка, чипсы, сухарики, сладости и соусы, которые содержат большое количество пищевых добавок, красителей, ароматизаторов, усилителей вкуса, консервантов и так далее. Е-добавки негативно влияют на весь организм в целом, в том числе и на органы зрения.
Быстрые углеводы — булочки, сладости, макароны и рафинированный рис. Они также вызывают повышенную выработку инсулина, к тому же негативно воздействуют на сетчатку глаза, вызывая ее разрушение.
Соль — она нужна организму, но только в ограниченных количествах — не более шести граммов в сутки. Избыточное количество соли задерживает выведение жидкости из организма и может повысить внутриглазное давление, что приведет к серьезным проблемам со зрением вплоть до катаракты.
К счастью, кроме вредных для зрения продуктов, есть еще продукты — защитники глаз.
— Прежде всего это витамины А, группы В и лютеин. За счет улучшения кровоснабжения они оказывают полезное действие на питание тканей сетчатки, прозрачность хрусталика. Ведь чем лучше обеспечение тканей глаза кровью и кислородом, тем меньше застойных явлений и ниже риск заболеваний глаз. А когда в рационе систематически не хватает витаминов А, В1 и РР (человек не ест рыбу, сливочное масло, яйца), снижается зрение в ситуации низкой освещенности, — говорит врач-диетолог «Федерального исследовательского центра питания, биотехнологии и безопасности пищи» Екатерина Бурляева.
Конечно, не стоит думать, что если человек каждый день будет есть только полезные для зрения продукты, то у него никогда не будет заболеваний глаз. Тем не менее глаза можно «подкормить». Для этого подойдет черника, морковь, сладкий перец, шпинат, брюссельская капуста.
— Рыба жирных сортов (лосось, скумбрия, сельдь). Тоже содержит витамин А, а также полиненасыщенные жирные кислоты.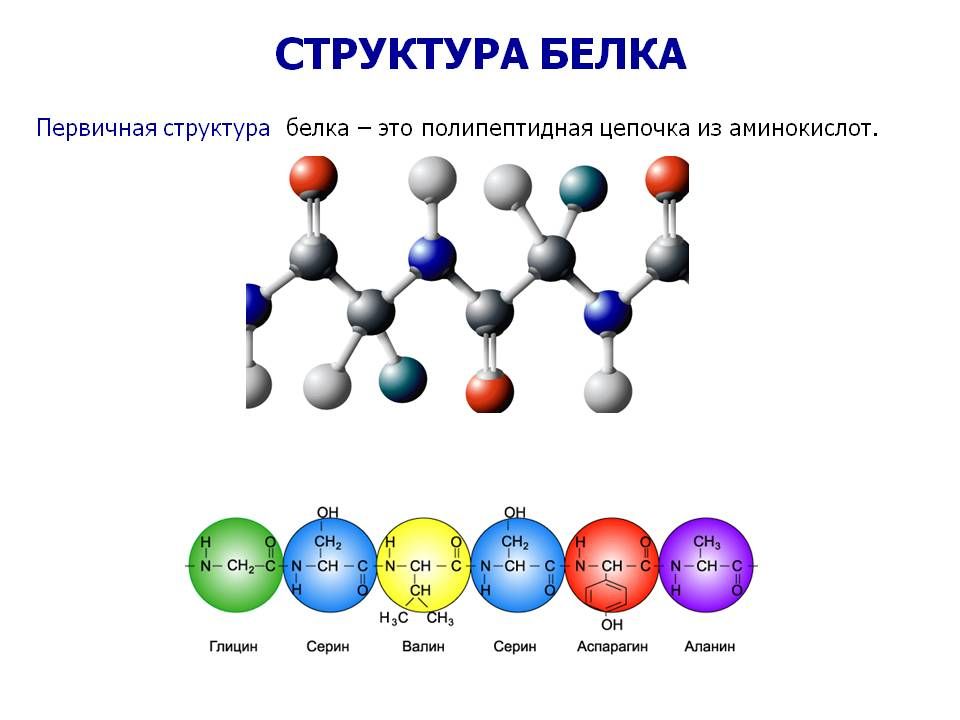 Аминокислоты (триптофан, лизин, таурин) способствуют нормальному функционированию глаз и нервной системы. Рыба, особенно красная, помогает для профилактики «синдрома сухого глаза». Регулярное употребление рыбы помогает сохранить остроту зрения в пожилом возрасте, способствуя защите от дегенеративных заболеваний сетчатки глаза. Не забывайте есть рыбу 2-3 раза в неделю, — считает Екатерина Бурляева.
Аминокислоты (триптофан, лизин, таурин) способствуют нормальному функционированию глаз и нервной системы. Рыба, особенно красная, помогает для профилактики «синдрома сухого глаза». Регулярное употребление рыбы помогает сохранить остроту зрения в пожилом возрасте, способствуя защите от дегенеративных заболеваний сетчатки глаза. Не забывайте есть рыбу 2-3 раза в неделю, — считает Екатерина Бурляева.
Аминокислоты Amino Magic Fuel 1000 ml MAXLER
Amino Magic Fuel 1000 ml MAXLER
Особенности Amino Magic Fuel (1000мл):
1. обогащен витамином B6
2. повышенная концентрация белка
3. жидкая форма для быстрого усвоения
4. приятный вкус
Amino Magic – это полный аминокислотный комплекс на основе коллагенового гидролизата, а также гидролизатов сывороточного и яичного белков. Кроме того, это — быстродействующий и легко усваиваемый источник L-карнитина, BCAA (лейцин, изолейцин, валин), аминокислот в форме пептидов и свободных аминокислот. Препарат также содержит стресс-комплекс витаминов группы В, холин и инозитол.
Amino Magic — аминокислоты премиум класса. Жидкая форма, позволяющая аминокислотам быстрее усваиваться, и повышенная концентрация белка делают Amino Magic действительно уникальным, «волшебным» продуктом. Прежде всего, высокая скорость усвоения при приеме до нагрузки и сразу после позволяет создавать, так называемый, «пул свободных аминокислот», который, в свою очередь, будет стимулировать анаболизм, иммунную систему, обмен веществ и восстановительные процессы. Amino Magic подходит для применения, как профессиональным спортсменам, так и начинающим атлетам.
Наиболее актуальным применение Maxler Amino Magic Fuel является для тех людей, которые предпочитают всякого рода силовые виды спорта. Ключевым элементом, входящим в состав препарата является коллагеновый белок. В его состав входят аминокислоты, благотворно влияющие на восстановление суставов, костных и соединительных тканей.
Maxler Amino Magic Fuel является действительно незаменимым средством для всех любителей спорта. Препарат обладает на редкость приятным вкусом, а также массой полезных свойств. Продукт усваивается в организме человека очень быстро, стимулирует обмен веществ, укрепляет иммунную систему, обеспечивает эффективность процессов восстановления.
Состав 1 порции (45мл):
Энергетическая ценность — 132,9 ккал
Белки — 18,0 г
ВСАА -1,5 г
Углеводы — 6,5 г
сахара — 6,5 г
Жиры — 0,0 г
насыщенные жирные кислоты <0,1г
Пищевые волокна — 0,0 г
Натрий < 0,1 г
Ниацин — 16,7 мг
Пантетовая кислота — 6,3 мг
Витамин В6 — 1,5 мг
Витамин В2 — 1,5 мг
Витамин В1 — 1,2 мг
Фолиеваz кислота — 210 мг
Биотин — 52 мкг
Витамин В12 — 2,6 мкг
Парааминобензойная кислота — 2,1 мг
Холина хлорид — 62,8 мг
L-карнитин — 26,1 мг
Инозит — 104,6 мг
Другие ингредиенты:
вода, гидролизованный желатин, фруктоза, кислотообразующие вещества (молочная кислота), мальтодекстрин, гидролизат сывороточного белка, гидролизат яичного белка, вкусовая добавка, загустители (карбоксиметил целюллоза, инозит), консервант сорбат калия), холина хлорид, Л-карнитин, ниацин, пантотеновая кислота, эмульгатор Е 471, парааминобензойная кислота, биотин, витамин В 6, витамин В1, витамин В 12.
Рекомендации по применению:
Одна порция аминокислот Amino Magic составляет 45 мл (3 столовые ложки). Учитывая высокую концентрацию белка в продукте, рекомендуется размешивать порцию Amino Magic с небольшим количеством воды. Прием аминокислот в обычные и тренировочные дни зависит от общей массы тела и суммарного количества употребляемого за день белка. При условии применения Amino Magic, как единственного высокобелкового продукта, общей рекомендацией по приему может служить: одна порция с утра натощак и по одной порции с каждым основным приемом пищи далее в течение дня. При условии комбинирования Amino Magic с другими высокобелковыми продуктами, количество порций должно высчитываться, исходя из суммарного количества потребленного за сутки белка.
При условии комбинирования Amino Magic с другими высокобелковыми продуктами, количество порций должно высчитываться, исходя из суммарного количества потребленного за сутки белка.
Фотогалерея молекулярных выражений
: Коллекция аминокислот
Заинтересованы в аминокислотах? Ознакомьтесь с нашей обширной фотогалереей аминокислот.
Аминокислоты — очень маленькие биомолекулы со средней молекулярной массой около 135 Дальтон (или единицы атомной массы, сокращенно AMU ). Эти органические кислоты существуют в природе в состоянии цвиттериона , где фрагмент карбоновой кислоты ионизирован, а основная аминогруппа протонирована.Весь класс аминокислот имеет общую основу, состоящую из группы органической карбоновой кислоты и аминогруппы, присоединенной к насыщенному атому углерода. Самым простым членом этой группы является глицин, в котором насыщенный атом углерода незамещен, что делает его оптически неактивным. Остальные 20 наиболее распространенных аминокислот являются оптически активными и существуют как стереоизомеры D и L . Встречающиеся в природе аминокислоты, которые включены в белки, по большей части являются левовращающим ( L ) изомером.Заместители у альфа (или насыщенного) атома углерода варьируются от низших алкильных групп до ароматических аминов и спиртов. Существуют также кислотные и основные боковые цепи, а также тиоловые цепи, которые могут окисляться до дитиольных связей между двумя подобными аминокислотами.
Валин
Аминокислоты являются основными строительными блоками белков и ферментов. Они включаются в белки с помощью РНК переноса в соответствии с генетическим кодом, в то время как РНК-мессенджер декодируется рибосомами.Во время и после окончательной сборки белка содержание аминокислот определяет пространственные и биохимические свойства белка или фермента. Аминокислотный каркас определяет первичную последовательность белка, но именно природа боковых цепей определяет свойства белка. Боковые цепи аминокислот могут быть полярными, неполярными или практически нейтральными. Полярные боковые цепи, как правило, присутствуют на поверхности белка, где они могут взаимодействовать с водной средой клеток.С другой стороны, неполярные аминокислоты обычно располагаются в центре белка, где они могут взаимодействовать с аналогичными неполярными соседями. Это может создать гидрофобную область внутри фермента, где химические реакции могут проводиться в неполярной атмосфере. Точно так же ферменты могут также иметь полярные аминокислотные заместители в активном центре, которые обеспечивают полярную область, в которой можно проводить биохимический синтез.
Боковые цепи аминокислот могут быть полярными, неполярными или практически нейтральными. Полярные боковые цепи, как правило, присутствуют на поверхности белка, где они могут взаимодействовать с водной средой клеток.С другой стороны, неполярные аминокислоты обычно располагаются в центре белка, где они могут взаимодействовать с аналогичными неполярными соседями. Это может создать гидрофобную область внутри фермента, где химические реакции могут проводиться в неполярной атмосфере. Точно так же ферменты могут также иметь полярные аминокислотные заместители в активном центре, которые обеспечивают полярную область, в которой можно проводить биохимический синтез.
Аланин
Помимо своей роли в синтезе белков и ферментов, аминокислоты активно участвуют в широком спектре функций организма.Например, органические вещества помогают формировать клетки, излечивать поврежденные ткани и вырабатывать антитела. Эти антитела важны для усилий организма по предотвращению потенциально вредоносных вторжений вирусов и бактерий. Также активные в качестве промежуточных продуктов метаболизма, аминокислоты способны переносить кислород по телу и играть роль в мышечной функции. Некоторые аминокислоты, такие как нейромедиатор гамма -аминомасляная кислота ( ГАМК ), которая содержится в центральной нервной системе, но не в белках, выполняют очень специфические роли в организме.Другие примеры таких аминокислот включают карнитин, который участвует в транспорте жирных кислот внутри клетки, а также орнитин и цитруллин, оба из которых являются ключевыми компонентами цикла мочевины в организме.
Лизин
Организм человека не может производить все 20 аминокислот, необходимых для синтеза белков. С пищей необходимо употреблять не менее 8 важных органических соединений, а две дополнительные аминокислоты (гистидин и аргинин) необходимы только детям.У других животных незаменимые аминокислоты несколько различаются. Например, в 1970-х годах у кошек было обнаружено, что у них отсутствует способность синтезировать таурин, аминокислоту, которая не считается необходимой для человека или другого любимого домашнего питомца — собаки.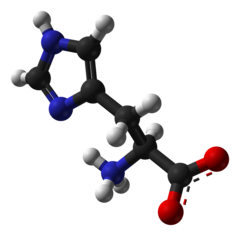 До этого открытия кошки часто страдали проблемами зрения, сердечными заболеваниями, циррозом и другими проблемами из-за диеты, в которой не было достаточного количества таурина. Однако с тех пор состав большинства брендов кормов для кошек был изменен, чтобы включать в себя достаточное количество аминокислоты.Симптомы действия аминокислоты у человека могут быть столь же серьезными, хотя точные эффекты зависят от того, каких соединений не хватает организму. Дефицит всех аминокислот характеризуется недоеданием, анемией и разрушением мышечной ткани.
До этого открытия кошки часто страдали проблемами зрения, сердечными заболеваниями, циррозом и другими проблемами из-за диеты, в которой не было достаточного количества таурина. Однако с тех пор состав большинства брендов кормов для кошек был изменен, чтобы включать в себя достаточное количество аминокислоты.Симптомы действия аминокислоты у человека могут быть столь же серьезными, хотя точные эффекты зависят от того, каких соединений не хватает организму. Дефицит всех аминокислот характеризуется недоеданием, анемией и разрушением мышечной ткани.
метионин
Незаменимые аминокислоты обычно содержатся в наибольшем количестве в мясе, птице, рыбе, яйцах и других продуктах животного происхождения. Однако они также содержатся в зернах, бобовых и аналогичных растительных источниках белка, хотя одна или несколько незаменимых аминокислот могут отсутствовать в таких продуктах.По этой причине вегетарианцам обычно рекомендуется тщательно потреблять широкий спектр продуктов, чтобы они регулярно получали полный набор незаменимых аминокислот, поскольку разные растения не имеют разных типов важных соединений. Тем не менее, дефицит аминокислот в Соединенных Штатах крайне редок, поскольку американцы обычно ежедневно потребляют в два раза больше белка, чем считается необходимым. Более того, для спортсменов или других людей, которым требуется большее количество аминокислот, чем большинству людей, широко доступны добавки.Некоторые аминокислоты даже назначаются в качестве лечебного средства. Лизин, например, используется для подавления вируса герпеса, а фенилаланин становится все более популярным при лечении боли и депрессии. Тем не менее, чрезмерное потребление аминокислот может быть опасным, поскольку соединения могут быть токсичными в чрезмерных количествах.
2.2: Структура и функции — аминокислоты
Источник: BiochemFFA_2_1.pdf. Весь учебник можно бесплатно получить у авторов по адресу http: // biochem.science.oregonstate.edu/content/biochemistry-free-and-easy
Все белки на Земле состоят из одних и тех же 20 аминокислот.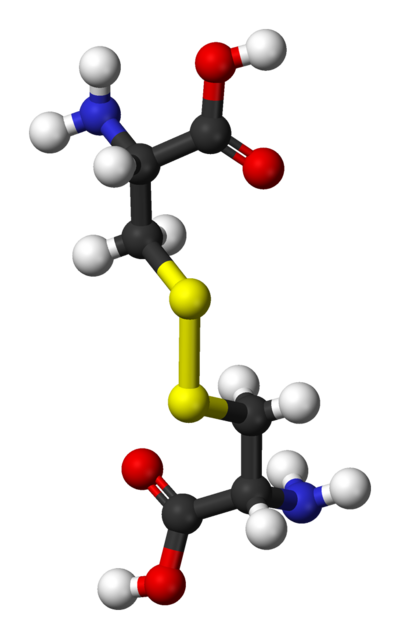 Связанные вместе в длинные цепи, называемые полипептидами, аминокислоты являются строительными блоками для огромного ассортимента белков, обнаруженных во всех живых клетках.
Связанные вместе в длинные цепи, называемые полипептидами, аминокислоты являются строительными блоками для огромного ассортимента белков, обнаруженных во всех живых клетках.
«Это одно из наиболее поразительных обобщений биохимии … что двадцать аминокислот и четыре основания, с небольшими оговорками, одинаковы во всей Природе.« — Фрэнсис Крик,
Все аминокислоты имеют одинаковую основную структуру, показанную на рисунке 2.1. В «центре» каждой аминокислоты находится углерод, называемый α углеродом, и к нему присоединены четыре группы — водород, α-карбоксильная группа, α-аминогруппа и R-группа, иногда называемая боковая цепь. Α-углеродная, карбоксильная и аминогруппы являются общими для всех аминокислот, поэтому R-группа является единственной уникальной особенностью каждой аминокислоты. (Незначительным исключением из этой структуры является пролин, в котором конец R-группы присоединен к α-амину.) За исключением глицина, который имеет R-группу, состоящую из атома водорода, все аминокислоты в белках имеют четыре разные группы, присоединенные к ним, и, следовательно, могут существовать в двух формах зеркального отображения, L и D. за небольшими исключениями, каждая аминокислота, обнаруженная в клетках и белках, имеет L-конфигурацию.
Рисунок 2.1 — Общая структура аминокислот
В белках содержатся 22 аминокислоты, из которых только 20 определены универсальным генетическим кодом.Другие, селеноцистеин и пирролизин, используют тРНК, которые способны образовывать пары оснований со стоп-кодонами в мРНК во время трансляции. Когда это происходит, эти необычные аминокислоты могут быть включены в белки. Ферменты, содержащие селеноцистеин, например, включают глутатионпероксидазы, тетрайодтиронин-5′-дейодиназы, тиоредоксинредуктазы, формиатдегидрогеназы, глицинредуктазы и селенфосфатсинтетазу. Белки, содержащие пирролизин, встречаются гораздо реже и в основном встречаются в архее.
Существенное и несущественное
Диетологи делят аминокислоты на две группы — незаменимые аминокислоты (должны присутствовать в рационе, потому что клетки не могут их синтезировать) и заменимые аминокислоты (могут производиться клетками). Эта классификация аминокислот имеет мало общего со структурой аминокислот. Незаменимые аминокислоты значительно различаются от одного организма к другому и даже различаются у людей, в зависимости от того, взрослые они или дети. В таблице 2.1 показаны незаменимые и заменимые аминокислоты в организме человека.
Эта классификация аминокислот имеет мало общего со структурой аминокислот. Незаменимые аминокислоты значительно различаются от одного организма к другому и даже различаются у людей, в зависимости от того, взрослые они или дети. В таблице 2.1 показаны незаменимые и заменимые аминокислоты в организме человека.
Некоторые аминокислоты, которые обычно не являются незаменимыми, в определенных случаях могут потребоваться из рациона. Людям, которые не синтезируют достаточное количество аргинина, цистеина, глутамина, пролина, селеноцистеина, серина и тирозина, например, из-за болезни, могут потребоваться пищевые добавки, содержащие эти аминокислоты.
Таблица 2.1 — Незаменимые и заменимые аминокислоты
Небелковые аминокислоты
Есть также α-аминокислоты, обнаруженные в клетках, которые не включены в белки.Общие включают орнитин и цитруллин. Оба эти соединения являются промежуточными продуктами цикла мочевины. Орнитин является метаболическим предшественником аргинина, а цитруллин может вырабатываться при расщеплении аргинина. Последняя реакция дает оксид азота, важную сигнальную молекулу. Цитруллин — это побочный продукт метаболизма. Иногда его используют в качестве пищевой добавки для снижения мышечной усталости.
Химия группы R
Таблица 2.2 — Категории аминокислот (на основе свойств R-группы)
Мы разделяем аминокислоты на категории на основе химического состава их R-групп.Если вы сравните группы аминокислот в разных учебниках, вы увидите разные названия категорий и (иногда) одну и ту же аминокислоту, классифицируемую разными авторами по-разному. Действительно, мы относим тирозин как к ароматической аминокислоте, так и к гидроксиламинокислоте. Полезно классифицировать аминокислоты на основе их R-групп, потому что именно эти боковые цепи придают каждой аминокислоте ее характерные свойства. Таким образом, можно ожидать, что аминокислоты с (химически) сходными боковыми группами будут функционировать аналогичным образом, например, во время сворачивания белка.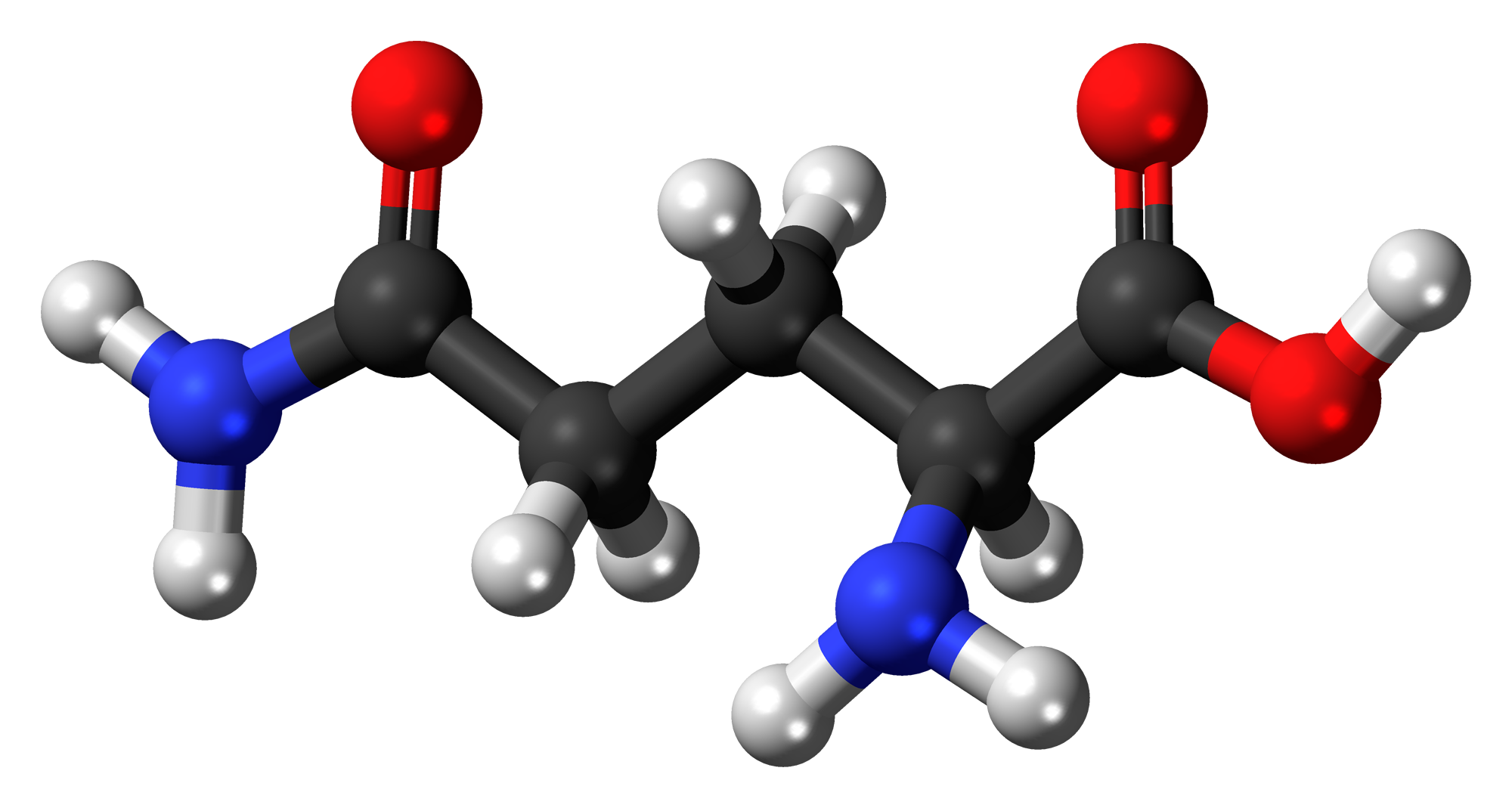
Неполярные аминокислоты
- Аланин (Ala / A) — одна из самых распространенных аминокислот, обнаруженных в белках, по распространенности уступающая только лейцину. D-форма аминокислоты также содержится в стенках бактериальных клеток. Аланин несущественен, легко синтезируется из пирувата. Он кодируется GCU, GCC, GCA и GCG.
- Глицин (Gly / G) — это аминокислота с самой короткой боковой цепью, имеющая R-группу, соответствующую только одному водороду. В результате глицин — единственная нехиральная аминокислота.Его небольшая боковая цепь позволяет ему легко вписываться как в гидрофобную, так и в гидрофильную среду.
Рисунок 2.2 — Свойства боковой цепи аминокислот Wikipedia
- Глицин определен в генетическом коде GGU, GGC, GGA и GGG. Для людей это несущественно.
- Изолейцин (Ile / I) — незаменимая аминокислота, кодируемая AUU, AUC и AUA. У него гидрофобная боковая цепь, а также хиральная боковая цепь.
- Лейцин (Leu / L) — это аминокислота с разветвленной цепью, гидрофобная и незаменимая.Лейцин является единственной диетической аминокислотой, которая, как сообщается, напрямую стимулирует синтез белка в мышцах, но следует соблюдать осторожность, поскольку 1) существуют противоречивые исследования и 2) токсичность лейцина опасна, что приводит к «четырем D»: диарее, дерматиту, деменции. и смерть. Лейцин кодируется шестью кодонами: UUA, UUG, CUU, CUC, CUA, CUG.
- Метионин (Met / M) — незаменимая аминокислота, которая является одной из двух серосодержащих аминокислот, цистеин — другой. Метионин неполярен и кодируется исключительно кодоном AUG.Это «инициатор» аминокислоты в синтезе белка, поскольку она первая включается в белковые цепи. В прокариотических клетках первый метионин в белке формилируется.
Рисунок 2.3 — Неполярные аминокислоты
- Пролин (Pro / P) — единственная аминокислота, обнаруженная в белках с R-группой, которая соединяется со своей собственной α-аминогруппой, образуя вторичный амин и кольцо.
 Пролин является незаменимой аминокислотой и кодируется CCU, CCC, CCA и CCG. Это наименее гибкая из аминокислот белка и, таким образом, придает конформационную жесткость, когда присутствует в белке.Присутствие пролина в белке влияет на его вторичную структуру. Это разрушитель α-спиралей и β-цепей. Пролин часто гидроксилирован в коллагене (для реакции требуется витамин С — аскорбат), что увеличивает конформационную стабильность белка. Гидроксилирование пролином фактора, индуцируемого гипоксией (HIF), служит датчиком уровня кислорода и направляет HIF на разрушение при избытке кислорода.
Пролин является незаменимой аминокислотой и кодируется CCU, CCC, CCA и CCG. Это наименее гибкая из аминокислот белка и, таким образом, придает конформационную жесткость, когда присутствует в белке.Присутствие пролина в белке влияет на его вторичную структуру. Это разрушитель α-спиралей и β-цепей. Пролин часто гидроксилирован в коллагене (для реакции требуется витамин С — аскорбат), что увеличивает конформационную стабильность белка. Гидроксилирование пролином фактора, индуцируемого гипоксией (HIF), служит датчиком уровня кислорода и направляет HIF на разрушение при избытке кислорода. - Валин (Val / V) — незаменимая неполярная аминокислота, синтезируемая в растениях.Это примечательно в отношении гемоглобина, поскольку, когда он заменяет глутаминовую кислоту в позиции номер шесть, он вызывает аномальную агрегацию гемоглобина в условиях низкого содержания кислорода, что приводит к серповидно-клеточной анемии. Валин закодирован в генетическом коде GUU, GUC, GUA и GUG.
Карбоксиламинокислоты
- Аспарагиновая кислота (Asp / D) — это незаменимая аминокислота с карбоксильной группой в R-группе. Он легко образуется при переаминировании оксалоацетата. При pKa 3,9 боковая цепь аспарагиновой кислоты отрицательно заряжена при физиологическом pH.Аспарагиновая кислота указана в генетическом коде кодонами GAU и GAC.
- Глутаминовая кислота (Glu / E), кодируемая GAA и GAG, представляет собой заменимую аминокислоту, легко получаемую путем трансаминирования α-кетоглутарата. Он является нейротрансмиттером и имеет R-группу с карбоксильной группой, которая легко ионизируется (pKa = 4,1) при физиологическом pH.
Рисунок 2.4 — Карбоксиламинокислоты
Аминокислоты
- Аргинин (Arg / R) — это аминокислота, которая в некоторых случаях является незаменимой, а в других — несущественной.Недоношенные дети не могут синтезировать аргинин. Кроме того, хирургическая травма, сепсис и ожоги увеличивают потребность в аргинине.
 Однако большинству людей добавки аргинина не нужны. Боковая цепь аргинина содержит сложную гуанидиниевую группу с pKa более 12, что делает ее положительно заряженной при клеточном pH. Он кодируется шестью кодонами — CGU, CGC, CGA, CGG, AGA и AGG.
Однако большинству людей добавки аргинина не нужны. Боковая цепь аргинина содержит сложную гуанидиниевую группу с pKa более 12, что делает ее положительно заряженной при клеточном pH. Он кодируется шестью кодонами — CGU, CGC, CGA, CGG, AGA и AGG. - Гистидин (His / H) — единственная из белковых аминокислот, которая содержит имидазольную функциональную группу. Это незаменимая аминокислота для человека и других млекопитающих.С pKa боковой цепи, равным 6, его заряд может легко измениться при небольшом изменении pH. Протонирование кольца приводит к двум структурам NH, которые можно представить как две одинаково важные резонансные структуры.
Рисунок 2.5 — Аминокислоты
- Лизин (Lys / K) — незаменимая аминокислота, кодируемая AAA и AAG. Он имеет группу R, которая может легко ионизироваться с зарядом +1 при физиологическом pH и может быть посттрансляционно модифицирована с образованием ацетиллизина, гидроксилизина и метиллизина.Он также может быть убиквитинирован, сумоилирован, неддилирован, биотинилирован, карбоксилирован и пупилирован, и. О-гликозилирование гидроксилизина используется для маркировки белков для экспорта из клетки. Лизин часто добавляют в корм для животных, поскольку он является ограничивающей аминокислотой и необходим для оптимизации роста свиней и цыплят.
Ароматические аминокислоты
Рисунок 2.6 — Ароматические аминокислоты
- Фенилаланин (Phe / F) — неполярная незаменимая аминокислота, кодируемая UUU и UUC.Это метаболический предшественник тирозина. Неспособность метаболизировать фенилаланин возникает из-за генетического нарушения, известного как фенилкетонурия. Фенилаланин входит в состав искусственного подсластителя аспартама.
- Триптофан (Trp / W) — незаменимая аминокислота, содержащая индольную функциональную группу. Это метаболический предшественник серотонина, ниацина и (в растениях) фитогормона ауксина. Несмотря на то, что он считается снотворным, четких результатов исследований, подтверждающих это, нет.

- Тирозин (Tyr / Y) — это незаменимая аминокислота, кодируемая UAC и UAU.Он является мишенью для фосфорилирования белков тирозиновыми протеинкиназами и играет роль в процессах передачи сигналов. В дофаминергических клетках мозга тирозингидроксилаза превращает тирозин в l-допа, непосредственный предшественник дофамина. Дофамин, в свою очередь, является предшественником норадреналина и адреналина. Тирозин также является предшественником гормонов щитовидной железы и меланина.
Гидроксиламинокислоты
- Серин (Ser / S) — одна из трех аминокислот, имеющих R-группу с гидроксилом в ней (другие — треонин и тирозин).Он кодируется UCU, UCC, UCA, UGC, AGU и AGC. Обладая водородной связью с водой, он классифицируется как полярная аминокислота. Для человека это несущественно. Серин является предшественником многих важных клеточных соединений, в том числе пуринов, пиримидинов, сфинголипидов, фолиевой кислоты и аминокислот глицина, цистеина и триптофана. Гидроксильная группа серина в белках является мишенью для фосфорилирования некоторыми протеинкиназами. Серин также является частью каталитической триады сериновых протеаз.
Рисунок 2.7 — Гидроксиламинокислоты
- Треонин (Thr / T) — полярная аминокислота, которая является незаменимой. Это одна из трех аминокислот, несущих гидроксильную группу (серин и тирозин — другие), и как таковая является мишенью для фосфорилирования белков. Он также является мишенью для гликозилирования белков. Треониновые протеазы используют гидроксильную группу аминокислоты в своем катализе, и она является предшественником одного пути биосинтеза для производства глицина. В некоторых случаях он используется в качестве пролекарства для повышения уровня глицина в мозге.Треонин кодируется в генетическом коде ACU, ACC, ACA и ACG.
Тирозин — см. ЗДЕСЬ.
Рисунок 2.8 — Свойства аминокислот Википедия
Другие аминокислоты
- Аспарагин (Asn / N) — это незаменимая аминокислота, кодируемая AAU и AAC.
 Его карбоксиамид в R-группе придает ему полярность. Аспарагин участвует в образовании акриламида в продуктах, приготовленных при высоких температурах (жарка во фритюре), когда он реагирует с карбонильными группами. Аспарагин может быть произведен в организме из аспартата путем реакции амидирования амином из глутамина.При распаде аспарагина образуется малат, который может окисляться в цикле лимонной кислоты.
Его карбоксиамид в R-группе придает ему полярность. Аспарагин участвует в образовании акриламида в продуктах, приготовленных при высоких температурах (жарка во фритюре), когда он реагирует с карбонильными группами. Аспарагин может быть произведен в организме из аспартата путем реакции амидирования амином из глутамина.При распаде аспарагина образуется малат, который может окисляться в цикле лимонной кислоты. - Цистеин (Cys / C) — единственная аминокислота с сульфгидрильной группой в боковой цепи. Это несущественно для большинства людей, но может быть необходимо для младенцев, пожилых людей и людей, страдающих определенными метаболическими заболеваниями. Сульфгидрильная группа цистеина легко окисляется до дисульфида при взаимодействии с другой группой. Цистеин не только содержится в белках, но и входит в состав трипептида, глутатиона.Цистеин определяется кодонами UGU и UGC.
Рисунок 2.9 — Другие аминокислоты
- Глютамин (Gln / Q) — это аминокислота, которая обычно не является незаменимой для людей, но может быть у людей, проходящих интенсивные спортивные тренировки или страдающих желудочно-кишечными расстройствами. Он имеет карбоксиамидную боковую цепь, которая обычно не ионизируется при физиологических значениях pH, но придает полярность боковой цепи. Глутамин кодируется CAA и CAG и легко образуется путем амидирования глутамата.Глютамин — самая распространенная аминокислота в циркулирующей крови и одна из немногих аминокислот, способных преодолевать гематоэнцефалический барьер.
- Селеноцистеин (Sec / U) — компонент селенопротеинов, обнаруженных во всех сферах жизни. Он является компонентом нескольких ферментов, включая глутатионпероксидазы и тиоредоксинредуктазы. Селеноцистеин включается в белки по необычной схеме, включающей стоп-кодон UGA. Клетки, выращенные в отсутствие селена, прекращают синтез белка на UGA.Однако, когда присутствует селен, некоторые мРНК, которые содержат последовательность вставки селеноцистеина (SECIS), вставляют селеноцистеин при обнаружении UGA.
 Элемент SECIS имеет характерные нуклеотидные последовательности и вторичные структуры спаривания оснований. Двадцать пять белков человека содержат селеноцистеин.
Элемент SECIS имеет характерные нуклеотидные последовательности и вторичные структуры спаривания оснований. Двадцать пять белков человека содержат селеноцистеин. - Пирролизин (Pyl / O) — двадцать вторая аминокислота, но редко встречается в белках. Как и селеноцистеин, он не закодирован в генетическом коде и должен быть включен необычными способами.Это происходит по стоп-кодонам UAG. Пирролизин содержится в метаногенных архейских организмах и, по крайней мере, в одной метан-продуцирующей бактерии. Пирролизин входит в состав ферментов, производящих метан.
Ионизирующие группы
Значения
pKa для боковых цепей аминокислот очень зависят от химической среды, в которой они присутствуют. Например, карбоксил R-группы, обнаруженный в аспарагиновой кислоте, имеет значение pKa 3,9 в свободном состоянии в растворе, но может достигать 14 в определенных средах внутри белков, хотя это необычно и экстремально.Каждая аминокислота имеет по крайней мере одну ионизируемую аминогруппу (α-амин) и одну ионизируемую карбоксильную группу (α-карбоксил). Когда они связаны пептидной связью, они больше не ионизируются. Некоторые, но не все аминокислоты имеют R-группы, которые могут ионизировать. Заряд белка тогда возникает из-за зарядов α-аминогруппы, α-карбоксильной группы. и сумма зарядов ионизированных R-групп. Титрование / ионизация аспарагиновой кислоты показано на рисунке 2.10. Ионизация (или деионизация) в структуре белка может иметь значительное влияние на общую конформацию белка и, поскольку структура связана с функцией, большое влияние на активность белка.
Рисунок 2.10 — Кривая титрования аспарагиновой кислоты Изображение Пенелопы Ирвинг
Большинство белков имеют относительно узкие диапазоны оптимальной активности, которые обычно соответствуют окружающей среде, в которой они находятся (рисунок 2.11). Стоит отметить, что образование пептидных связей между аминокислотами удаляет ионизируемые водороды как из α-аминных, так и из α-карбоксильных групп аминокислот. Таким образом, ионизация / деионизация в белке происходит только от 1) аминоконца; 2) карбоксильный конец; 3) R-группы; или 4) другие функциональные группы (такие как сульфаты или фосфаты), добавленные к аминокислотам посттрансляционно — см. ниже.
Таким образом, ионизация / деионизация в белке происходит только от 1) аминоконца; 2) карбоксильный конец; 3) R-группы; или 4) другие функциональные группы (такие как сульфаты или фосфаты), добавленные к аминокислотам посттрансляционно — см. ниже.
Карнитин
Не все аминокислоты в клетке находятся в белках. Наиболее распространенные примеры включают орнитин (метаболизм аргинина), цитруллин (цикл мочевины) и карнитин (рис. 2.12). Когда жирные кислоты, предназначенные для окисления, перемещаются в митохондрии с этой целью, они перемещаются через внутреннюю мембрану, прикрепленную к карнитину. Из двух стереоизомерных форм L-форма является активной. Молекула синтезируется в печени из лизина и метионина.
Фигура 2.12 — L-карнитин
Из экзогенных источников жирные кислоты должны активироваться при попадании в цитоплазму путем присоединения к коферменту A. Часть CoA молекулы заменяется карнитином в межмембранном пространстве митохондрии в реакции, катализируемой карнитином. ацилтрансфераза I. Полученная в результате молекула ацилкарнитина переносится через внутреннюю митохондриальную мембрану карнитинацилкарнитинтранслоказой, а затем в матриксе митохондрии карнитинацилтрансфераза II заменяет карнитин коферментом А (рис.88).
Рисунок 2.11 — Активность фермента изменяется при изменении pH Изображение Aleia Kim
Катаболизм аминокислот
Мы классифицируем аминокислоты как незаменимые и несущественные в зависимости от того, может ли организм их синтезировать. Однако все аминокислоты могут расщепляться всеми организмами. Фактически, они являются источником энергии для клеток, особенно во время голодания или для людей, соблюдающих диету с очень низким содержанием углеводов. С точки зрения распада (катаболизма) аминокислоты классифицируются как глюкогенные, если они производят промежуточные соединения, которые могут быть превращены в глюкозу, или кетогенные, если их промежуточные соединения превращаются в ацетил-КоА.На рис. 2.13 показана метаболическая судьба катаболизма каждой из аминокислот. Обратите внимание, что некоторые аминокислоты являются как глюкогенными, так и кетогенными.
Обратите внимание, что некоторые аминокислоты являются как глюкогенными, так и кетогенными.
Рисунок 2.13 — Катаболизм аминокислот. У некоторых есть более одного пути. Изображение Пера Якобсона
Пост-трансляционные модификации
После того, как белок синтезирован, боковые цепи аминокислот в нем могут быть химически модифицированы, что приведет к большему разнообразию структуры и функций (рис. 2.14). Общие изменения включают фосфорилирование гидроксильных групп серина, треонина или тирозина.Лизин, пролин и гистидин могут иметь гидроксильные группы, добавленные к аминам в их R-группах. Другие модификации аминокислот в белках включают добавление жирных кислот (миристиновой кислоты или пальмитиновой кислоты), изопреноидных групп, ацетильных групп, метильных групп, йода, карбоксильных групп или сульфатов. Они могут иметь эффекты ионизации (добавление фосфатов / сульфатов), деионизации (добавление ацетильной группы к амину R-группы лизина) или вообще не влиять на заряд. Кроме того, N-связанные и O-связанные гликопротеины содержат углеводы, ковалентно присоединенные к боковым цепям аспарагина и треонина или серина соответственно.
Некоторые аминокислоты являются предшественниками важных соединений в организме. Примеры включают адреналин, гормоны щитовидной железы, Ldopa и дофамин (все из тирозина), серотонин (из триптофана) и гистамин (из гистидина).
Рисунок 2.14 — Посттрансляционно модифицированные аминокислоты. Изменения показаны зеленым цветом. Изображение Пенелопы Ирвинг Рисунок 2.15 — Фосфорилированные аминокислоты
Строительные полипептиды
Хотя аминокислоты выполняют в клетках и другие функции, их наиболее важная роль заключается в том, что они являются составными частями белков.Белки, как мы уже отмечали ранее, представляют собой полимеры аминокислот.
Аминокислоты связаны друг с другом пептидными связями, в которых карбоксильная группа одной аминокислоты соединяется с аминогруппой следующей с потерей молекулы воды.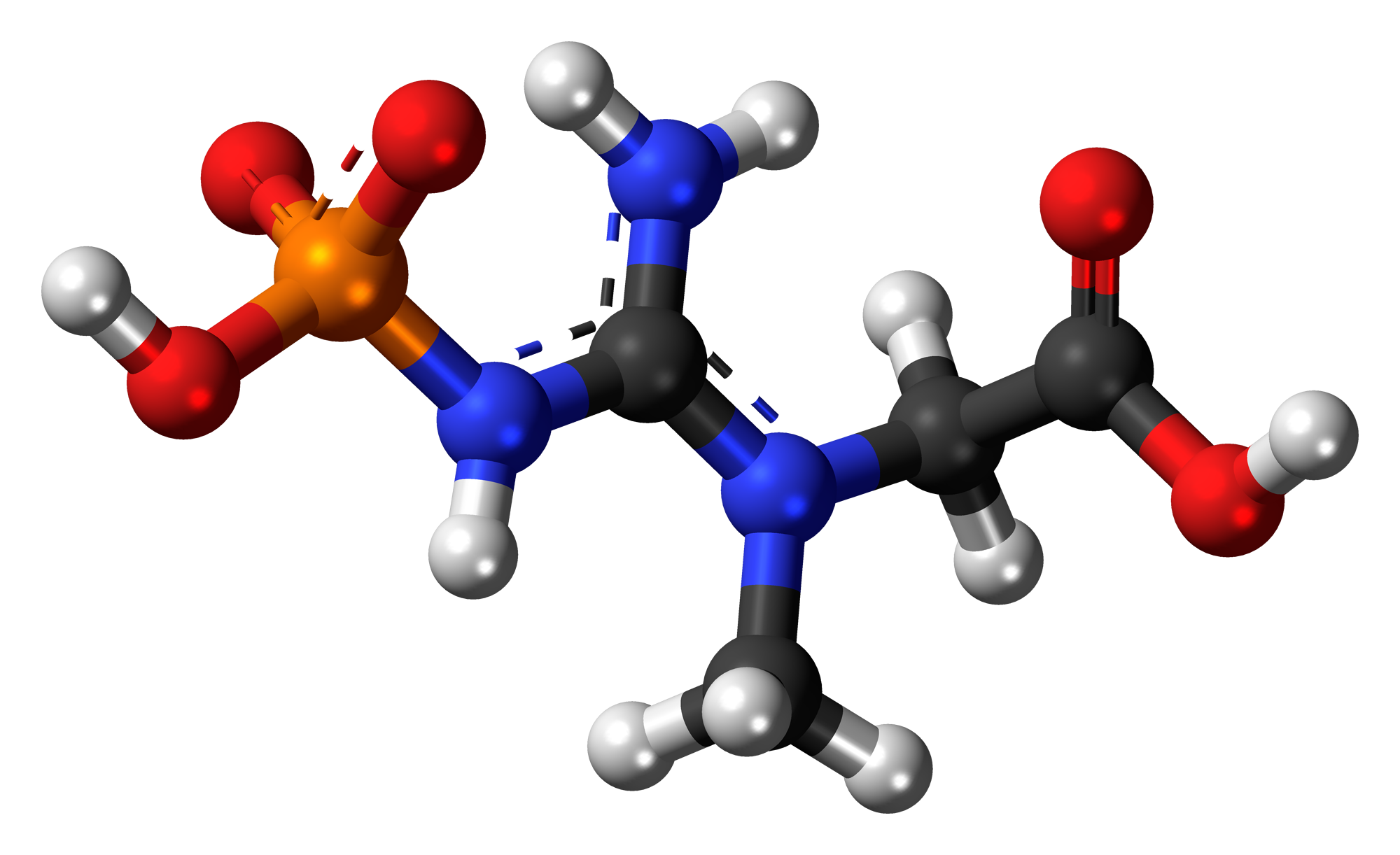 Дополнительные аминокислоты добавляются таким же образом путем образования пептидных связей между свободным карбоксилом на конце растущей цепи и аминогруппой следующей аминокислоты в последовательности. Цепь, состоящая всего из нескольких связанных вместе аминокислот, называется олигопептидом (олиго = несколько), а типичный белок, состоящий из множества аминокислот, называется полипептидом (поли = много).Конец пептида, который имеет свободную аминогруппу, называется N-концом (для Nh3), а конец со свободным карбоксилом называется C-концом (для карбоксила).
Дополнительные аминокислоты добавляются таким же образом путем образования пептидных связей между свободным карбоксилом на конце растущей цепи и аминогруппой следующей аминокислоты в последовательности. Цепь, состоящая всего из нескольких связанных вместе аминокислот, называется олигопептидом (олиго = несколько), а типичный белок, состоящий из множества аминокислот, называется полипептидом (поли = много).Конец пептида, который имеет свободную аминогруппу, называется N-концом (для Nh3), а конец со свободным карбоксилом называется C-концом (для карбоксила).
Рис. 2.16. Формирование пептидной связи
Как мы уже отмечали ранее, функция зависит от структуры, и цепочка аминокислот должна складываться в определенную трехмерную форму или конформацию, чтобы образовался функциональный белок. Сворачивание полипептидов в их функциональные формы — тема следующего раздела.
Анализаторы аминокислот помогают в поиске новых биотерапевтических средств
Устойчивость бактерий к антибиотикам увеличивается, о чем свидетельствует эта чашка Петри, обработанная градиентом активности антибиотика.© Родольфо Парулан-младший/Moment/Getty Images
Растущее количество биологических препаратов, получающих одобрение регулирующих органов по всему миру, привело к значительному сдвигу в направлении открытия и разработки новых терапевтических белков и пептидов. Успех моноклональных антител для лечения таких заболеваний, как рак, воспаление и аутоиммунные расстройства, а также пептидных препаратов для лечения метаболических нарушений и хронической боли демонстрирует, как биологические препараты произвели революцию в терапии трудноизлечимых заболеваний.
В настоящее время в глобальных клинических исследованиях находится более 400 пептидных препаратов, и более 60 уже одобрены для клинического использования в США, Европе и Японии. Рост в этом секторе, вероятно, продолжится, поскольку биохимики исследуют активность соединений из растущего разнообразия природных источников.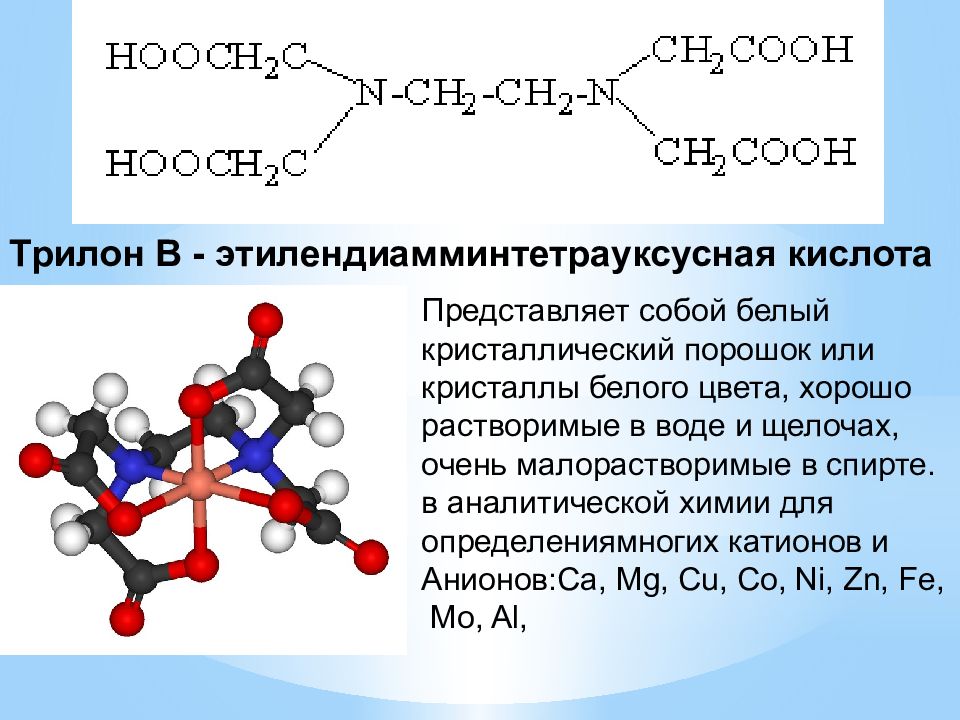
Традиционно открытие пептидных лекарств было сосредоточено на пептидах, уже обнаруженных в организме человека, но по мере того, как все больше патогенов и рака становятся устойчивыми к лекарствам, исследователи ищут биологически активные вещества из более экзотических источников.
«Чтобы найти новые натуральные продукты с различными механизмами антибиотической или противоопухолевой активности, мы должны искать биологическое разнообразие, предпочтительно на уровне рода или выше», — говорит доцент Керри Макфейл, структурный химик из Университета штата Орегон. Она путешествовала по миру в поисках филогенетически разнообразных и уникальных организмов из редких или экстремальных экосистем, которые производят новые лекарственные соединения.
Идентификация и очистка таких соединений — непростая задача.Он включает фракционирование экстрактов организмов и их тестирование в анализах для определения их биологической активности. Образцы, которые показывают многообещающие уровни активности, должны затем пройти множество раундов очистки, чтобы получить биоактивное соединение. «Работа с очень ограниченным количеством образцов и определение трехмерной структуры биоактивного пептида, которая имеет решающее значение для его функции, являются серьезными проблемами», — объясняет Макфейл.
Сопоставляя данные тандемной масс-спектрометрии жидкостной хроматографии высокого разрешения (ЖХ-МС / МС) с результатами анализа активности, исследователи теперь могут получить структурную информацию на ранней стадии.Это позволяет им определять приоритеты, какие образцы анализировать, и избегать дублирования работы с соединениями, которые могут быть уже известны.
Тогда, когда дело доходит до их массового производства без потери активности, необходимо преодолевать дополнительные препятствия. Технологии, обеспечивающие высокопроизводительный и точный анализ аминокислот в биоактивных пептидах, не только способствуют валидации протоколов очистки, но также удовлетворяют потребность в последовательном производстве биологических препаратов и контроле качества.
Анализаторы аминокислот предоставляют качественную и количественную информацию об аминокислотном составе гидролизата белка или пептида с помощью непрерывной проточной ионообменной жидкостной хроматографии, метода, первоначально разработанного Спакманом, Муром и Стейном в 1958 году в Институте медицинских исследований Рокфеллера ( Нью-Йорк). С тех пор внедрение методов автоматизации и улучшение ионообменных смол значительно сократили время анализа.
Высокоскоростной анализатор аминокислот модели LA8080 © Hitachi High-Technologies
Hitachi совершенствует характеристики и конструкцию анализаторов аминокислот с 1962 года.Последняя модель, высокоскоростной анализатор аминокислот LA8080 AminoSAAYA, обеспечивает точную идентификацию и количественное определение аминокислот с высокой чувствительностью обнаружения и, что особенно важно, с низким расходом образцов.
«Предоставляя точные концентрации исходных пептидов или белка, LA8080 может помочь исследователям охарактеризовать биотерапевтические препараты», — говорит Масахито Ито, ведущий разработчик технологии.
LA8080 отличается от предыдущих моделей тем, что он был разработан для размещения на стандартном лабораторном столе, что упрощает замену реагентов и настройку образца.«Это большая разница, — говорит Ито. «Это удобнее в использовании, компактнее и надежнее».
Его компактный дизайн уменьшил его размер примерно на 30% по сравнению с предшественниками, но, что важно, LA8080 AminoSAAYA совместим с методами, используемыми на предыдущих моделях (L-8800 / L-8900). «Основные аналитические условия, колонки (упаковочные материалы) и реагенты можно продолжать использовать без каких-либо изменений», — объясняет Ито.
Масахито Ито, ведущий разработчик технологии Hiatchi High-Tech Science Corporation, стоит перед своим новейшим анализатором аминокислот LA8080, объясняя его функции.© Hitachi High-Technologies
Помимо анализа биоактивных пептидов, LA8080 может использоваться для анализа физиологических жидкостей, что важно для понимания фармакодинамики и фармакокинетики лекарств, а также среды для культивирования клеток для оптимизации условий длительного роста. LA8080 использовался для определения концентрации дипептида 1-аланил-1-глутамина (AlaGln) в среде для культивирования клеток. «В отличие от глутамина, который разлагается в культуральной среде и производит токсичный продукт аммоний, AlaGln очень стабилен в водных растворах и является желательной добавкой в среду для выращивания клеток млекопитающих с дефицитом гена глутамина», — объясняет Ито.
Текущие усилия по созданию больших хранилищ натуральных продуктов и пониманию взаимосвязи структура-активность в пептидах, вероятно, будут стимулировать спрос на точный аминокислотный анализ при открытии и разработке биотерапевтических лекарств.
«Мы собрали множество натуральных продуктов, и только сейчас мы можем тестировать их в исчезающе малых количествах», — говорит Макфейл.
Подробнее: LA8080 История продукта »
Этот рекламный ролик подготовлен компанией Nature Research Custom Media для Hitachi High-Technologies.Рекламодатель сохраняет ответственность за содержание. Об этом содержании .
Почему 20 аминокислот? | Feature
Для многих исследователей изучение химического происхождения жизни — это побочный проект — это то, чем они занимаются в перерывах между финансируемыми грантами работой по изучению причин и лечению болезней человека. Но понимание эволюции на химическом уровне — их страсть, даже когда финансирование скудно. Как химия могла привести нас к сложной жизни, вызывает много открытых вопросов.Один из фундаментальных вопросов — почему жизнь основана на наборе 20 аминокислот. Почему 20, а не 10 или 30? А почему именно эти 20? За последние несколько десятилетий увлеченные химики и молекулярные биологи, которые не могут оставить эти вопросы в покое, начали собирать воедино некоторые убедительные объяснения.
От аланина (A) до тирозина (Y), 20 «протеиногенных» аминокислот, каждая из которых обозначается аббревиатурой с разными буквами, составляют алфавитный суп жизни. Они являются строительными блоками для белков, макромолекул «рабочей лошадки» биологии, которые обеспечивают структуру и функции всех организмов.Но почему аминокислоты? Бернд Моосманн, эксперт по окислительно-восстановительной медицине из Университета Йоханнеса Гутенберга в Майнце в Германии, предполагает, что первые аминокислоты были использованы для закрепления мембран в структурах РНК: «Вы можете увидеть это даже в современной жизни: ДНК и РНК в бактериях и митохондриях всегда присутствуют. прикреплены изнутри к мембране. » Большинство исследователей считают, что это могло произойти по крайней мере 4 миллиарда лет назад в ‘мире РНК’, где молекулы РНК были первыми саморепликаторами, а также выполняли каталитическую роль, которую играют белки. Cегодня.
Как протеиногенные аминокислоты появились на Земле — еще один важный вопрос. Знаменитый эксперимент Миллера-Юри 1952 года показал, что с помощью электрических искр, имитирующих молнию, простые соединения, такие как вода, метан, аммиак и водород, образуют более 20 различных аминокислот. 1 Они также встречаются в метеоритах: анализ метеорита Меричисон, приземлившегося в Австралии в 1969 году, обнаружил по крайней мере 86 аминокислот, цепи заместителей, содержащие до девяти атомов углерода, а также дикарбоксильные и диаминофункциональные группы. 2 Может быть, эти в общем простые и легко доступные аминокислоты были первыми, кто претворялся в жизнь?
Эндрю Дойг, химический биолог из Манчестерского университета в Великобритании, размышлял о химии эволюции, когда не проводил свои исследования болезни Альцгеймера. У него другой взгляд на этот вопрос: «[Протеиногенные аминокислоты] были выбраны в мире РНК, где миллионы лет существовала жизнь и метаболизм, которые уже генерировали огромное количество органических молекул.«Если бы аминокислоты были продуктом метаболизма РНК, это бы значительно увеличило их концентрацию в окружающей среде», — утверждает он.
Но выбор из 20 аминокислот, используемых в биологии, явно связан с развитием белков. Путем полимеризации аминокислот в длинных полипептидных цепях белки могут складываться в растворимые структуры с плотно упакованными ядрами и упорядоченными связывающими карманами. Появление белков и, в конечном итоге, принятие 20 стандартных аминокислот, вероятно, было большим эволюционным шагом.
Но, по словам Дойга, это все домыслы. «У нас вообще нет прямых доказательств». Из сравнения геномов организмов сегодня мы знаем, что 3,5–3,8 миллиарда лет назад наш общий предок, известный как последний универсальный общий предок, использовал 20 общих для всех аминокислот. живые существа.
Замерзшая авария?
Так почему именно этот набор из 20 аминокислот, а не какие-либо другие? «Очевидным недостатком является способность проводить окислительно-восстановительные реакции», — объясняет Дойг.«Они не были выбраны из-за способности выполнять катализ напрямую». Сегодня белки образуют ферменты для биологического катализа, но первыми биологическими катализаторами в мире РНК, вероятно, были то, что мы сейчас называем кофакторами — ионы металлов или небелковые органические молекулы. (коферменты), которые помогают ферментам в катализе реакций и часто состоят из витаминов.
Существовала тенденция рассматривать выбор из 20 аминокислот как произвольный — как в «теории замороженных аварий», предложенной британским молекулярным биологом Фрэнсисом Криком в 1960-х годах, который предполагал, что другая группа из 20 будет столь же хорошей.«Я продолжал читать это и понимал, что это неправильно, — говорит Дойг. Это побудило его изложить свои мысли в недавней статье, где он утверждает, что есть причины, по которым выбор каждой аминокислоты делает их почти идеальной группой. 3 Факторы, которые он учел, включали атомы, функциональные группы каждой аминокислоты и стоимость биосинтеза.
Для формирования растворимых, стабильных белковых структур с плотно упакованными ядрами и упорядоченными связывающими карманами требовалось то разнообразие аминокислот, которое мы видим сегодня, — объясняет Дойг.Необходимы множественные гидрофобные белки. «Ядро белка — это трехмерная головоломка — если у вас много разных гидрофобных аминокислот, это дает вам больше возможностей построить ядро без каких-либо промежутков».
Тот факт, что гидрофобные аминокислоты обычно имеют разветвленные боковые цепи, также можно объяснить. Внутри белкового ядра молекула больше не может вращаться и теряет часть связанной с ней энтропии. «Если у вас есть разветвленные аминокислоты, такие как валин, лейцин и изолейцин, вы теряете меньше энтропии, когда закапываете их, поэтому эволюция выбрала гидрофобные аминокислоты не только потому, что они гидрофобны, но и потому, что они разветвленные», — объясняет Дойг.«Если вы хотите, чтобы аминокислоты входили в ядро белка, вы делаете его разветвленным и гидрофобным, если вы хотите, чтобы он был на поверхности, вы делаете его с прямой цепью и полярным, как аргинин и глутаминовая кислота».
Химическое пространство
Стивен Фриланд, астробиолог из Университета Мэриленда в США, разработал метод, показывающий, что аминокислоты, принятые биологией, не были выбраны случайным образом. Он позаимствовал идею химического пространства из открытия лекарств, где молекулы нанесены в трехмерное пространство, чтобы помочь обнаружить бреши, которые могут открыть новые молекулы лекарств.Фриланд и его команда исследовали три параметра: размер, заряд и гидрофобность. «Они не идеальны, — признает Фриланд, — но в качестве приблизительных показателей того, что делают аминокислоты и почему они это делают, эти три довольно хороши». Гидрофобность, очевидно, играет ключевую роль в том, как белки складываются, заряд важен в реакциях и Активные сайты и размер интуитивно понятны, говорит Фриланд.
«Мы обнаружили, что набор, который используется биологией, обладает рядом удивительно неслучайных свойств, которые очень четко выделяются», — говорит Фриланд.Аминокислоты были широко распределены по своему химическому пространству, но также показали равномерность в этом распределении — как будто пытались охватить как можно больше различных наборов свойств. 4 «То, что мы обнаруживаем с [протеиногенными] аминокислотами, — это момент, когда вы добавляете оба этих фактора [гидрофобность и заряд], почти каждый тест, который вы можете провести с ними, говорит, что они неслучайны — не только они покрывают хороший диапазон, но они не сгущаются в крайности ».
Итак, если этот неслучайный набор аминокислот был выбран по уважительной причине, можно ли создать порядок, в котором они были включены в биологию? «Сейчас все согласны с тем, что не все они пришли сразу, что, на мой взгляд, подавляюще», — говорит Фриланд.Попытка дать исчерпывающий заказ была предпринята израильским молекулярным биофизиком Эдвардом Трифоновым, который сейчас работает в Институте эволюции Хайфского университета. Трифонов открыл множество новых кодов в ДНК и в начале 2000-х обратил свое внимание на аминокислоты.
Размещение простейших по химическому составу аминокислот в первую очередь может показаться очевидным, но Трифонов пошел дальше. Он рассмотрел несколько критериев, включая энергетические затраты на их синтез, тип молекул транспортной РНК, используемых для их транспортировки, и количество кодонов (последовательность из трех нуклеотидов РНК, которая соответствует определенной аминокислоте), используемых в синтезе белка; аминокислоты с несколькими кодонами, вероятно, старше, чем с одним.Он усреднил данные и предложил временной порядок, начиная с аланина и глицина. 5
Freeland также рассмотрел, как шаблоны могут изменяться в зависимости от аминокислот, которые, как предполагается, были приняты раньше и позже. Используя только первые 10 в химическом пространстве, он обнаружил неслучайные свойства в отличие от изучения всех возможных аминокислот, доступных на пребиотической земле (от Миллера-Юри или метеоритов). Затем он добавил полный набор из 20. «Более поздние из них расширяют химическое пространство первых таким образом, чтобы максимизировать диапазон и равномерность, и для моих денег наиболее интересным является то, что они, кажется, закрывают область химического пространства, которая была раньше. малонаселенный, между тем, где сидят самые ранние, и тем, где будут сидеть димеры самых ранних », — говорит он.«Совершенно логично, что именно сюда можно подключать».
Oxygen расширяет код
Мы, конечно, знаем, что белки могут быть получены из гораздо меньшего набора аминокислот. Японская группа, возглавляемая Сатоши Аканума из Университета Васэда, недавно показала, что алфавит из 13 аминокислот может создавать свернутые, растворимые, стабильные и каталитически активные «белки», хотя и не такие активные или стабильные, как исходные белки, на которых они основаны. 6 Итак, что могло побудить к добавлению дополнительных аминокислот? По словам Моосманна, молекулярный кислород заставил жизнь включить последние шесть новых аминокислот.
Предполагаемые последние шесть аминокислот (гистидин, фенилаланин, цистеин, метионин, триптофан и тирозин) все химически «мягче» — они сильно поляризуемы и связываются ковалентно. «Скорее всего, это адаптация, а не совпадение или дрейф», — говорит Моосманн. Эта идея пришла к Мосманну во время исследований ткани мозга мышей (его «повседневная работа» включает исследования нейродегенеративных заболеваний). Он заметил, что некоторые аминокислоты гораздо более склонны к окислительной деградации — те, которые, как считается, были приняты позже.
Если эти аминокислоты были добавлены в биологию из-за их окислительно-восстановительной активности, он догадывался, что эти адаптации связаны с повышением уровня молекулярного кислорода на Земле. Считается, что кислород стал частью окружающей среды Земли около 2,5 миллиардов лет назад в результате так называемого «великого окислительного события», но Моосманн говорит, что основная причина местного образования низких доз кислорода, вероятно, старше. Согласно недавнему исследованию эволюции ферментов, участвующих в фотосинтезе, Танай Кардона из Имперского колледжа Лондона в Великобритании предположил, что происхождение оксигенного фотосинтеза было 3.6 миллиардов лет назад. 7
Он решил продолжить исследование, изучив пробелы Homo – Lumo для всех биологических аминокислот. Энергетическая щель между самой высокой занятой молекулярной орбиталью и самой низкой незанятой молекулярной орбиталью предсказывает реакционную способность соединения по отношению к переносу электрона. 8 «Разрывы Homo – Lumo [из всех 20 аминокислот] имели закономерность, просто падая в той самой точке (номер 14), когда проявились« адаптивные »свойства, и это совпадение, вероятно, не совпадение!»
Значительно меньшие пробелы, обнаруженные для более поздних аминокислот, предполагают, что их основная функция заключалась в проведении окислительно-восстановительных реакций, и Мосманн утверждает, что это было необходимо в среде, где могли образовываться свободные радикалы кислорода, которые особенно разрушительны для липидов.«Более мягкие» и более окислительно-восстановительные аминокислоты были способны защищать клетки: «Эти [новые аминокислоты] могут поддерживать целостность липидного бислоя в присутствии повышающихся концентраций кислорода или в присутствии химических воздействий, которые имеют тенденцию атаковать или разлагают ненасыщенные жирные кислоты », — говорит Мосманн. «Для последних трех [метионин, триптофан и тирозин] есть неопровержимые доказательства реакции на кислород».
Тогда возникает один вопрос: содержал ли наш последний универсальный общий предок полный набор аминокислот.Исследование 2016 года выявило набор из 355 генов, предположительно присутствующих в организме, который стал известен как Лука. 9 Моосман говорит, что Лука датируется от 3,7 до 2,9 миллиарда лет назад, так что, возможно, кислород был доступен. «Следствием этого действительно является то, что Лука (если он когда-либо существовал) имел менее 20 аминокислот.» Он предполагает, что более поздние добавления генетического кода могли быть распределены латерально по всем современным линиям: «Я думаю, что у Луки было 17– 18 АК, без метионина, триптофана и, возможно, тирозина.’
Зачем останавливаться на 20?
Адаптация к насыщенному кислородом мире может объяснить расширение кода до 20 аминокислот, но зачем на этом останавливаться? «Я бы сказал, посмотрите, на что способны 20», — говорит Фриланд. «По-видимому, 20 — этого достаточно, чтобы почти каждый живой организм приспособился к невообразимому количеству сред обитания за всю историю жизни».
На самом деле, в организмах используются по крайней мере две дополнительные аминокислоты, хотя только одна из них содержится в человеческих белках — селенсодержащий селеноцистеин.Он обнаружен в активных центрах 25 белков человека, но включается более сложным механизмом, чем нормальный синтез белка. «Это показывает, что процесс не остановился, он достиг точки, когда внедрение новых аминокислот чрезвычайно сложно», — говорит Луис Рибас, молекулярный биолог из Института исследований биомедицины, Барселона, Испания. «Если вы хотите это сделать, вам нужно найти очень оригинальные решения».
Ограничение в распознавании тРНК
Чтобы ответить на вопрос «Почему 20?», Риблас внимательно изучил механизм синтеза белка — трансляцию.Процесс осуществляется в рибосоме клетки, очень большом комплексе молекул РНК и белка. Каждая аминокислота переносится специальной молекулой транспортной РНК (тРНК), присоединенной через гидроксильную группу с образованием сложного эфира. Затем он вступает в реакцию с концевой аминокислотой растущей белковой цепи. Правильная аминокислотная последовательность транслируется из молекул информационной РНК посредством спаривания оснований Уотсона – Крика с молекулами тРНК. Каждая тРНК содержит последовательности из трех оснований, специфичных для одной из 20 аминокислот — кодона.
Учитывая, что каждая аминокислота кодируется последовательностью из трех оснований, вы можете предположить, что существует 64 возможных комбинации (из четырех возможных оснований). Хотя три кодона используются в качестве инструкций для остановки синтеза белка, остается 61 — так зачем же останавливаться на 20 уникальных аминокислотах? «Ограничение заключается в распознавании тРНК», — говорит Рибас. Каждая молекула тРНК имеет четко определенную третичную структуру, которая распознается ферментом аминоацил тРНК синтетазой, который добавляет правильную аминокислоту.Изучая структуры тРНК, Рибас пришел к выводу, что проблема заключается в поиске способов создания новых молекул тРНК, которые могли бы распознавать новую аминокислоту, не подбирая существующие. 10 Возможные структуры ограничены, поскольку они также должны соответствовать существующему механизму трансляции белков.
‘Это как если бы у вас был очень простой тип замка, в котором вы могли бы заменить только три или четыре штифта, вы подошли к точке, где вы не сможете создавать новые ключи, потому что новый ключ откроет замок, который у вас уже есть используется, и это противоречит цели », — поясняет он.Точка, в которой природа не смогла создать новые уникальные тРНК, которые нельзя было бы принять за другие, по-видимому, находилась на уровне 20 аминокислот. В современной биологии это позволяет кодировать большинство аминокислот более чем одним кодоном — избыточность помогает более точной трансляции (по оценкам, ошибки включения аминокислот возникают один раз на 1000–10 000 кодонов).
Расширение кода аминокислоты
Рибас говорит, что его работа также имеет значение для синтетических биологов, которые пытаются продвинуть генетический код на шаг вперед, включив в него неестественные аминокислоты и, возможно, однажды улучшив природу.В 2011 году группа, в состав которой входил гарвардский биолог-синтетик Джордж Черч, удалила один из трех стоп-кодонов из бактерий E. coli , чтобы его можно было заменить альтернативной непротеиногенной аминокислотой, а другие лаборатории включили такие аминокислоты в белки.
Эволюционная теория говорит нам, что набор, который у нас есть, — это микрокосм возможного.
Но Рибас не уверен, что это будет успешная стратегия для синтетических биологов.«Если вы попытаетесь разработать систему in vivo для генерации белков с неестественными аминокислотами, она окажется не очень эффективной, низкая эффективность и часто возникают проблемы со специфичностью», — говорит он. Рибас объясняет это трудностью создания новых молекул тРНК в рамках существующего механизма трансляции белков. «Я не думаю, что есть какой-то способ обойти это, [без] обширной модернизации всего оборудования», хотя, добавляет он, в настоящее время это делается.
Даже если это станет возможным, Фриланд считает, что преимуществ будет мало.«Все в эволюционной теории говорит нам, что набор, который у нас есть, — это микрокосм того, что возможно». Окажется ли полезное применение у расширения жизненного репертуара аминокислот, еще предстоит увидеть, но сейчас есть много доказательств того, что 20 аминокислот Life были выбраны правильно, а не «замороженной случайностью».
Но Фриланд предостерегает от понимания, которое стремится аккуратно упорядочить химическую эволюцию. Скорее всего, когда-то это было намного сложнее, с вовлечением множества различных типов молекул и механизмов, которые, возможно, теперь были заменены.« Так заманчиво продвигаться от ничего к чему-то, потому что именно это происходит, когда химик садится со стаканом дистиллированной воды и пытается вызвать реакцию — но это не то, что происходит во Вселенной, Вселенная полон беспорядочной химии. ‘
Рэйчел Бразилия, научный писатель из Лондона, Великобритания.
(PDF) Изображения кристаллов аминокислот с молекулярным разрешением с помощью атомно-силового микроскопа
Перепечатано из Nature, Vol.332, No. 6162, pp. 332-334, 24 марта 1988 г.
Macmillan Magazines L td., 1988
Изображения с молекулярным разрешением кристаллов аминокислот
с помощью атомно-силового микроскопа
Скот Гулд *, О. Марти *, Барни Дрейк *,
Луи Хеллеманс *, Чарльз Э. Брекер *,
Пол К. Хансма *, Нэнси Л. Кедер§, Майкл М. Эдди§
и Гален Д. Стаки§
* Департамент наук, Калифорнийский университет, Санта-Барбара,
Калифорния 93106, США
Химический факультет Левенского университета, B-3030, Хеверли,
Бельгия
Департамент ботаники и патологии растений, Университет Пердью,
Запад Лафайет, Индиана 47907, США
§ Химический факультет Калифорнийского университета, Санта-Барбара,
Калифорния 93106, США
Атомно-силовой микроскоп использовался для изображения массивов из
молекул на поверхности кристаллов DL-лейцина. .Расстояние между решетками
согласуется с данными дифракции рентгеновских лучей. В отличие от металлов
и полупроводников, поверхность этих кристаллов аминокислот
кажется простым завершением основной массы; нет никаких доказательств реконструкции поверхности
для этого молекулярного кристалла. Этот первоначальный успех
в визуализации молекул аминокислот указывает на потенциальную
полезность атомно-силовой микроскопии для визуализации молекул
биологической важности.
За два года с момента изобретения атомно-силовой микроскоп Micro-
(AFM) 1 уже превратился в мощный аналитический прибор
. Он был использован для получения изображений с атомным разрешением
графита2-4 и других слоистых и неслоистых материалов
5,6, для изображения молекул в органическом монослое7,
для изучения деталей трения с атомным разрешением4, для обозначения —
электронных материалов8, а для изображения магнитных материалов — даже
записывающей головки магнитного устройства9.Он работает на принципах
, как и его предшественник, сканирующий туннельный микроскоп
(STM) 10, отображая контуры поверхностей, но
, тогда как STM требует образца, который будет проводить электроны
трона. AFM можно использовать с образцами
изолирующими или проводящими.
По сути атомно-силовой микроскоп работает как рекордный проигрыватель
. Наконечник прижимается к поверхности образца с прижимным усилием
в минуту ~ 10-8 Н и сканирует его.Изображения
состоят из серии сканирований, каждое из которых смещено от
предыдущего на небольшое расстояние, обычно 0,01 нм для изображений
, показанных здесь. Визуализация образца при этих крошечных усилиях слежения
, похоже, не повреждает поверхность, поскольку одну и ту же поверхность
можно сканировать многократно без изменения изображения.
Сердцем атомно-силового микроскопа является датчик силы
. Во всех атомных силовых микроскопах, которые были построены на сегодняшний день 1-9
, сила измерялась путем измерения отклонения
маленькой пружины с жесткостью пружины в диапазоне 0.1-100 Н
м-1. Для изображений в этой статье пружина представляла собой консоль
, изготовленную из позолоченной вольфрамовой проволоки диаметром
20 мкм. Консоль имела форму буквы «V»; каждая сторона была
длиной 1,4 мм, а заостренный фрагмент расколотого алмаза
был установлен на вершине буквы «V», чтобы действовать как зондирующий наконечник
, который контактировал с поверхностью образца. Жесткость пружины
составляла ~ 6 Н
м-1.
Прогиб кантилевера был измерен путем обнаружения
тока туннелирования электронов между вольфрамовой проволокой и
покрытым платиной лезвием бритвы, которое было расположено с механическими и пьезоэлектрическими элементами
на небольшом расстоянии позади консоли
3. .Для изображений в этом отчете лезвие бритвы было расположено под номером
таким образом, чтобы отклонение кантилевера составляло ~ 1 нм.
Силы, таким образом, составили ~ 6x 10-9 Н. Все представленные изображения — это
переменного туннельного тока между лезвием бритвы и
пружиной (режим переменного отклонения). Это сопоставимо с режимом постоянной высоты
, используемым со сканирующими туннельными микроскопами
. Контур медленной обратной связи отрегулировал положение образца
таким образом, чтобы средний туннельный ток (и, следовательно, среднее отклонение кантилевера
) оставался постоянным.
Для подготовки образцов кристаллические хлопья DL-лейцина (Cal-
biochem No. 4320) были прикреплены к кусочкам (~ 5×5 мм) стекла
предметного стекла микроскопа с небольшим количеством цианакрила, заполняющего зазоры,
поздний клей и хранится в эксикаторе, когда не используется. Открытая грань кристаллов
была получена непосредственно в воздухе с помощью АСМ
.
Фиг. 1 представляет собой АСМ-изображение DL-лейцина с линейным сканированием, на котором каждая молекула
выглядит как небольшой холмик.В каждом ряду видно около восьми молекул
. Расстояние между насыпями
~ 0,5 нм. На рис. 2 показано изображение образца DL-лейцина
в шкале серого, полученное на другом атомно-силовом микроскопе в нашей лаборатории. На этом изображении каждая молекула представлена в виде светлого пятна
на более темном фоне.
Рентгенограмма образца, приготовленного для АСМ
исследований, была записана на дифрактометре Scintag 6-6 (рис.
3). DL-лейцин кристаллизуется 11-12 в триклинной пространственной группе P1,
с параметрами решетки a = 0,539, b = 1,412, c = 0,519 нм,
97,0 °, = 111,1 °, = 86,4 °. Дифракционная картина показывает серию
пиков с 2 интервалами по 6,26 ° (CuK, A = 0,15418 нм), что соответствует
отражениям 0k0. Таким образом, отображаемая грань кристалла
параллельна плоскости a-c элементарной ячейки.
Пакет молекулярной графики CHEMX был использован для создания
упакованной кристаллической структуры из опубликованных кристалло-
графических данных 11-12.Исследование структуры, параллельной плоскости
ac, показывает, что наиболее вероятной точкой расщепления является
между метильными группами лейцина (рис. 4), а не
функциональные группы аминокислот на другом конце молекулы
, потому что силы Ван-дер-Ваальса между слоями
неполярных групп в кристалле намного слабее, чем водородная связь
, которая удерживает вместе двойной слой карбоксила и
аминогрупп.
Мы можем оценить некоторые параметры элементарной ячейки по нашим изображениям
АСМ, но необходимо принять во внимание источники ошибок. Температурный дрейф, недостаточная поперечная жесткость кантилевера, наклонные поверхности
и погрешность калибровки пьезоэлектрических элементов способствуют погрешности измерения
. Наклонные поверхности уменьшают измеренные расстояния
ниже истинных значений, тогда как недостаточная поперечная жесткость
увеличивает измеренные расстояния
Рис.1 Линейное изображение АСМ кристалла DL-лейцина (фото
, график исходных данных с экрана осциллографа). Курганы имеют размер
из-за того, что наконечник атомно-силового микроскопа просматривает более
отдельных молекул лейцина.
Premasol — не содержащий сульфитов (аминокислот) — изображения, изображения, этикетки | Уровень здоровья
Этикетка на контейнере
ЛОТ
EXP
2B0009
NDC 0338-1130-04
1000 мл
10% PREMASOL —
без сульфитов
(аминокислота) для инъекций
10%
Аптечная массовая упаковка
Не для прямой инфузии
Только рецепт
Каждые 100 мл содержат незаменимые аминокислоты ЛЕЙЦИН 1.4 г ИЗОЛЕУЦИН 0,82 г
ЛИЗИН 0,82 г (ДОБАВЛЕННЫЙ В КАЧЕСТВЕ ЛИЗИНА-АЦЕТАТА) ВАЛИН 0,78 г ГИСТИДИН 0,48 г
ФЕНИЛАЛАНИН 0,48 г ТРЕОНИН 0,42 г МЕТИОНИН 0,34 г ТИРОЗИН 0,24 г
(ДОБАВЛЕННЫЙ В КАЧЕСТВЕ ТИРОЗИНА И Н-ТРИОЗИНА 20) г
ЦИСТЕИН <0,016 г (ДОБАВЛЕН В КАЧЕСТВЕ ЦИСТИНА HClh3O)
Заменимые аминокислоты АРГИНИН 1,2 г ПРОЛИН 0,68 г АЛАНИН 0,54 г
ГЛУТАМИНОВАЯ КИСЛОТА 0,50 г СЕРИЯ 0,38 г ГЛИЦИНА 0,36 г АСПАРТИЧЕСКАЯ КИСЛОТА С ГЛЮЦИНАМИ 0,32 г
УКСУСНАЯ КИСЛОТА pH 5.5 (5.0-6.0)
ОСМОЛЯРНОСТЬ 865 мОсмоль / л (CALC)
мэкв / л АЦЕТАТ 94 ХЛОРИД <3 (CALC) СТЕРИЛ НЕПИРОГЕННЫЙ
НЕ СОДЕРЖИТ БОЛЕЕ 25 мкг / л ДОБАВЛЕННОГО АЛЮМИНИЯ
ЖИДКОСТЬ, НАПИСАННАЯ ИЗ
, В ЭТОМ КОНТЕЙНЕРЕ, ПОСМОТРЕТЬ С ФАРМАЦИСТОМ, ЕСЛИ ДОСТУПНО
, КОГДА ИСПОЛЬЗУЕТСЯ АСЕПТИЧЕСКАЯ ТЕХНИКА. КОНТЕЙНЕРЫ ПОЛИВИНИЛХЛОРИДА (ПВХ), В КОТОРЫХ ИСПОЛЬЗУЕТСЯ ФТАЛАТ ДИ-2-ЭТИЛГЕКСИЛА
(ДЭГФ) В КАЧЕСТВЕ ПЛАСТИФИКАТОРА, ПОТОМУ ЧТО ЖИРОВАЯ ЭМУЛЬСИЯ
ОБЕСПЕЧИВАЕТ ВЫЩИЩЕНИЕ ДЕГПА ИЗ ЭТИХ КОНТЕЙНЕРОВ
ДЛЯ ИСПОЛЬЗОВАНИЯ ACC
ПРОВЕРЬТЕ МИНУТУ УТЕЧЕК, НАЖИМАЯ СУМКУ.
ПОСЛЕ ЗАКРЫТИЯ КОНТЕЙНЕРА ИЗВЛЕЧЕНИЕ СОДЕРЖИМОГО
ДОЛЖНО БЫТЬ ЗАВЕРШЕНО БЕЗ ЗАДЕРЖКИ НЕ ИСПОЛЬЗУЙТЕ, ЕСЛИ РЕШЕНИЕ ПРОЗРАЧНО И УПЛОТНЕНИЕ НЕ ПОВРЕЖДЕНО
БЕЛЫЙ ЖЕЛТЫЙ ЦВЕТ НЕ МЕНЯЕТ КАЧЕСТВО И ЭФФЕКТИВНОСТЬ ПРОДУКТА
КОНТЕЙНЕР VIAFLEX
PL 146 ПЛАСТИК
Baxter Logo
BAXTER DEALTH IL 60015 USA
СДЕЛАНО В США
BAXTER PREMASOL PL 146 И
VIAFLEX ЯВЛЯЮТСЯ ТОВАРНЫМИ МАРКАМИ
BAXTER INTERNATIONAL INC
TERNATIONAL INC
Этикетка на картонной коробке
Лот: PXXXXXX
Exp: XXXXXXX
КОЛ-ВО: 12-1000 мл
Код: 2B0009
NDC: 0338-1130-04
10% акмасол — сульфит ) INJ
Контейнер Viaflex
(17) XXXXX00 (10) PXXXXXX
(01) 50303381130041
LOT EXP
2B0011 500 мл
NDC 0338-1131-03
6% PREMASOL — без сульфитов
(аминокислота) для инъекций
6%
Аптечный пакет для массовых грузов
Не для прямого вливания
Только Rx
КАЖДЫЙ 100 мл СОДЕРЖИТ ОСНОВНЫЕ АМИНОКИСЛОТЫ
ЛЕЙЦИН 0.84 г ИЗОЛЕУЦИН 0,49 г ЛИЗИН 0,49 г (ДОБАВЛЕН В КАЧЕСТВЕ ЛИЗИНАЦЕТАТА
) ВАЛИН 0,47 г ГИСТИДИН 0,29 г
ФЕНИЛАЛАНИН 0,29 г ТРЕОНИН 0,25 г МЕТИОНИН 0,20 г
ТИРОЗИН 0,14 г (ДОБАВЛЕН В КАЧЕСТВЕ ТИРОЗИНА И ЛОПАНАЦЕТИНА) 900 0,12 г ЦИСТЕИНА <0,014 г (ДОБАВЛЕН В КАЧЕСТВЕ ЦИСТЕИНА
HClh3O) НЕОБХОДИМЫЕ АМИНОКИСЛОТЫ АРГИНИН 1,2 г
PROLINE 0,41 г АЛАНИН 0,32 г ГЛУТАМИНОВАЯ КИСЛОТА 0,30 г СЕРИЯ
0,23 г ГЛИЦИН 0,22 г АСПАРАЧНАЯ КИСЛОТА С АУСТЕТОМ 0,015 г ГЛИЦИНА ТАУРИНА 0,22 г С АСУСТИЧЕСКОЙ КИСЛОТОЙ 0,015 г
ТАУРИН КИСЛОТА
pH 5.5 (5,0-6,0) ОСМОЛЯРНОСТЬ 520 мОсмоль / л (CALC)
мэкв / л АЦЕТАТ 57 ХЛОРИД <3 (CALC)
СТЕРИЛ НЕПИРОГЕННЫЙ
СОДЕРЖИТ НЕ БОЛЕЕ 25 мкг / л алюминия
ДОБАВИТЬ БЕДЕР E FLUID
, НАХОДЯЩИЙСЯ ИЗ ДАННОГО КОНТЕЙНЕРА, ОБРАЩАЙТЕСЬ С ФАРМАСИСТОМ
, ЕСЛИ ДОСТУПНО, ПРИ ПРИСОЕДИНЕНИИ ПРИСОЕДИНЕНИЙ
ИСПОЛЬЗУЙТЕ СМЕСЬ АСЕПТИЧЕСКОЙ ТЕХНИКИ ВСЕГДА
НЕ ХРАНИТЕ ДОЗИРОВКУ
ДЛЯ ВНУТРЕННЕЙ ДЕЗИРОВКИ ВНУТРЕННЕГО АДМИНИСТРАТОРА АДМИНИЗАТА
AS
. КОНТЕЙНЕРЫ ХЛОРИДА
(ПВХ), В КОТОРЫХ ИСПОЛЬЗУЕТСЯ ДИ-2-ЭТИЛГЕКСИЛФТАЛАТ
(ДЭГФ) В КАЧЕСТВЕ ПЛАСТИФИКАТОРА, ПОТОМУ ЧТО ЖИРОВАЯ ЭМУЛЬСИЯ
ОБЕСПЕЧИВАЕТ ВЫЩИЩЕНИЕ ДЭГПА ИЗ ЭТИХ КОНТЕЙНЕРОВ КОМПАНИИ DI-2-ЭТИЛГЕКСИЛФТАЛАТ
(ДЭГФ).
ПРИ ЗАКРЫТИИ КОНТЕЙНЕРА ВЫВОД
СОДЕРЖИМОГО ДОЛЖЕН БЫТЬ ЗАВЕРШЕН БЕЗ ЗАДЕРЖКИ
AFFIX СООТВЕТСТВУЮЩАЯ ЭТИКЕТКА ДАТЫ И ВРЕМЕНИ ЗАПИСИ
РАЗДАВАЙТЕ СОДЕРЖИМОЕ В ТЕЧЕНИЕ 4 ЧАСОВ ПОСЛЕ ПЕРВОНАЧАЛЬНОЙ ЗАПИСИ
ВНИМАНИЕ НЕ ИСПОЛЬЗУЙТЕ, ЕСЛИ РЕШЕНИЕ ЯЗОНО И ПЕЧАТЬ НЕ ПОВРЕЖДЕНЫ
БЛАГОРОДНЫЙ ЖЕЛТЫЙ ЦВЕТ НЕ МЕНЯЕТ КАЧЕСТВО И ЭФФЕКТИВНОСТЬ ПРОДУКТА
В
PL 146 PLASTIC
Baxter Logo
BAXTER HEALTHCARE CORPORATION
CLINTEC NUTRITION DIVISION
DEERFIELD IL 60015 USA СДЕЛАНО В США
BAXTER PREMASOL PL 146 И
VIAFLEX ЯВЛЯЮТСЯ МЕЖДУНАРОДНЫМИ ТОВАРНЫМИ МАРКАМИ
BAX, INC.
Лот: PXXXXXX Exp: XXXXXXX
КОЛ-ВО: 24/5000 мл Код: 2B0011
NDC: 0338-1131-03
6% Premasol — без сульфитов (аминокислот) INJ
Viaflex Container
(17) XXXXX00 (17) XXXXX00 (17) 10) PXXXXXX
(01) 50303381131031
06.03.09 14:20:03
Аминокислоты | BioNinja
Понимание:
• В полипептидах, синтезированных на рибосомах
, есть 20 различных аминокислот.
Белки состоят из длинных цепочек повторяющихся мономеров, называемых аминокислотами
Все аминокислоты имеют общую основную структуру с центральным атомом углерода, связанным с:
- Аминная группа (NH 2 )
- Карбоновая кислота группа (COOH)
- Атом водорода (H)
- Вариабельная боковая цепь (R)
Структура обобщенной аминокислоты
Существует 20 различных аминокислот, которые являются универсальными для всех живых организмов
- Еще две — селеноцистеин и пирролизин — являются модифицированными вариантами, обнаруженными только у определенных организмов
Понимание:
• Аминокислоты могут быть связаны друг с другом в любой последовательности, что дает огромный диапазон возможных полипептидов
Аминокислоты соединяются на рибосоме с образованием длинных цепей, называемых полипептидами , которые составляют белки
Каждый тип аминокислот отличается по составу вариабельной боковой цепи
Эти боковые цепи будут иметь различные химические свойства ( е.




 Это его основная роль. Но также лизин участвует в синтезе гормонов, антител, восстановлении тканей. Он хорошо влияет на работу сердца, усиливает сопротивляемость организма вирусам и снижает уровень триглицеридов, содержащихся в крови. Источниками этой аминокислоты является мясо птицы и говядины, а также горох и фасоль.
Это его основная роль. Но также лизин участвует в синтезе гормонов, антител, восстановлении тканей. Он хорошо влияет на работу сердца, усиливает сопротивляемость организма вирусам и снижает уровень триглицеридов, содержащихся в крови. Источниками этой аминокислоты является мясо птицы и говядины, а также горох и фасоль. Хорошими источниками этой аминокислоты является любое мясо, сыр и молоко.
Хорошими источниками этой аминокислоты является любое мясо, сыр и молоко. Набор продуктов, в которых содержится эта аминокислота, стандартен: молоко, мясо, яйца, рыба.
Набор продуктов, в которых содержится эта аминокислота, стандартен: молоко, мясо, яйца, рыба.
 Пролин является незаменимой аминокислотой и кодируется CCU, CCC, CCA и CCG. Это наименее гибкая из аминокислот белка и, таким образом, придает конформационную жесткость, когда присутствует в белке.Присутствие пролина в белке влияет на его вторичную структуру. Это разрушитель α-спиралей и β-цепей. Пролин часто гидроксилирован в коллагене (для реакции требуется витамин С — аскорбат), что увеличивает конформационную стабильность белка. Гидроксилирование пролином фактора, индуцируемого гипоксией (HIF), служит датчиком уровня кислорода и направляет HIF на разрушение при избытке кислорода.
Пролин является незаменимой аминокислотой и кодируется CCU, CCC, CCA и CCG. Это наименее гибкая из аминокислот белка и, таким образом, придает конформационную жесткость, когда присутствует в белке.Присутствие пролина в белке влияет на его вторичную структуру. Это разрушитель α-спиралей и β-цепей. Пролин часто гидроксилирован в коллагене (для реакции требуется витамин С — аскорбат), что увеличивает конформационную стабильность белка. Гидроксилирование пролином фактора, индуцируемого гипоксией (HIF), служит датчиком уровня кислорода и направляет HIF на разрушение при избытке кислорода. Однако большинству людей добавки аргинина не нужны. Боковая цепь аргинина содержит сложную гуанидиниевую группу с pKa более 12, что делает ее положительно заряженной при клеточном pH. Он кодируется шестью кодонами — CGU, CGC, CGA, CGG, AGA и AGG.
Однако большинству людей добавки аргинина не нужны. Боковая цепь аргинина содержит сложную гуанидиниевую группу с pKa более 12, что делает ее положительно заряженной при клеточном pH. Он кодируется шестью кодонами — CGU, CGC, CGA, CGG, AGA и AGG.
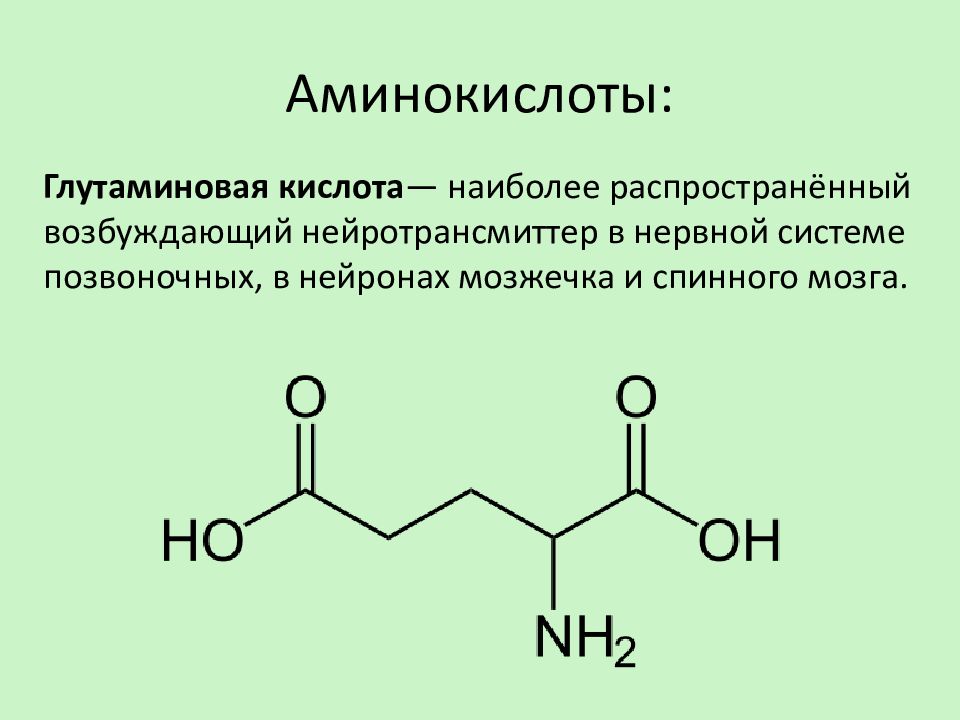 Его карбоксиамид в R-группе придает ему полярность. Аспарагин участвует в образовании акриламида в продуктах, приготовленных при высоких температурах (жарка во фритюре), когда он реагирует с карбонильными группами. Аспарагин может быть произведен в организме из аспартата путем реакции амидирования амином из глутамина.При распаде аспарагина образуется малат, который может окисляться в цикле лимонной кислоты.
Его карбоксиамид в R-группе придает ему полярность. Аспарагин участвует в образовании акриламида в продуктах, приготовленных при высоких температурах (жарка во фритюре), когда он реагирует с карбонильными группами. Аспарагин может быть произведен в организме из аспартата путем реакции амидирования амином из глутамина.При распаде аспарагина образуется малат, который может окисляться в цикле лимонной кислоты. Элемент SECIS имеет характерные нуклеотидные последовательности и вторичные структуры спаривания оснований. Двадцать пять белков человека содержат селеноцистеин.
Элемент SECIS имеет характерные нуклеотидные последовательности и вторичные структуры спаривания оснований. Двадцать пять белков человека содержат селеноцистеин.