Таблица названия аминокислот: Таблица аминокислот
2. Аминокислоты
Аминокислоты
– органические
гетерофункциональные соединения,
молекулы которых содержат одновременно
амино- (–NH2)
и карбоксильную
(–COOH)
группы. Общая формула:
где
m
– число аминогрупп, а n
– число карбоксильных групп. В более
широком смысле к аминокислотам могут
быть отнесены и соединения с иной
кислотной функцией, например,
аминосульфоновые кислоты.
Классификация
аминокислот
По числу
функциональных (амино и карбоксильных)
групп:
моноаминомонокарбоновые;
диаминомонокарбоновые;
аминодикарбоновые
и т. д.
От природы
углеводородного радикала аминокислоты:
ароматические
гетероциклические
От взаимного
расположения амино- и карбоксильной
групп:
По отношению
к биологическим организмам:
Заменимые.

Синтезируются
в организме человека. К ним относятся
глицин, аланин, глутаминовая кислота,
серин, аспарагиновая кислота, тирозин,
цистеин.Незаменимые.
Не синтезируются
в организме человека в количествах,
достаточных для того, чтобы удовлетворить
физиологические потребности организма,
поступают с пищей.
Номенклатура
аминокислот.
Простейшим соединением ряда аминокислот
является глицин
NH2–CH2–COOH.
Для названия
аминокислот используют следующие
номенклатуры:
тривиальная;
рациональная;
систематическая.
Тривиальная.
Родоначальники гомологических рядов
алифатических и ароматических аминокислот
– глицин и аминобензойная кислота
соответственно. Происхождение этих
Происхождение этих
исторических названий связано со
свойствами и названиями продуктов, из
которых они впервые были выделены.
Глицин имеет сладкий вкус, впервые был
выделен из «животного клея» (от греч.
glycos
– сладкий и kolla
– клей и произошло название гликокол).
Цистин выделен из камней желчного пузыря
(от греч. «цистис» – пузырь). Лейцин
получен из молочного белка – казеина
(от греч. «леукос»
– белый). Аспарагиновая кислота
изолирована от ростков спаржи (от греч.
«аспарагус»
– спаржа). Орнитин выделен из помёта
птиц (от греч. «орнитус»
– птица).
Рациональная.
Производится
путём прибавления к названию соответствующей
карбоновой кислоты (название кислоты
используется тривиальное), приставки
амино-. Буквой греческого алфавита
указывается положение аминогруппы по
отношению к карбоксильной группе.
Систематическая
номенклатура.
Название производится от названия
соответствующей карбоновой кислоты с
указанием местоположения аминогруппы
и заместителей при помощи локантов.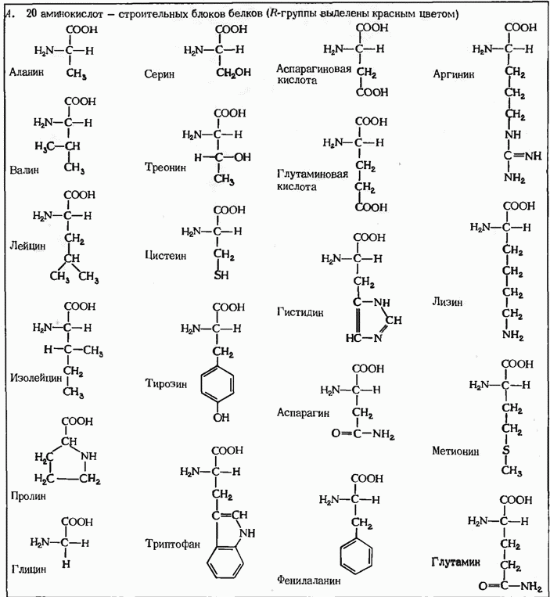 В
В
названиях алифатических аминокислот
по заместительной номенклатуре
аминогруппа обозначается префиксом
амино-,
а карбоксильная группа как старшая –
суффиксом —овая
кислота. В названиях ароматических
аминокислот в качестве родоначальной
структуры используется бензойная
кислота. Для аминокислот, участвующих
в построении белков, применяются в
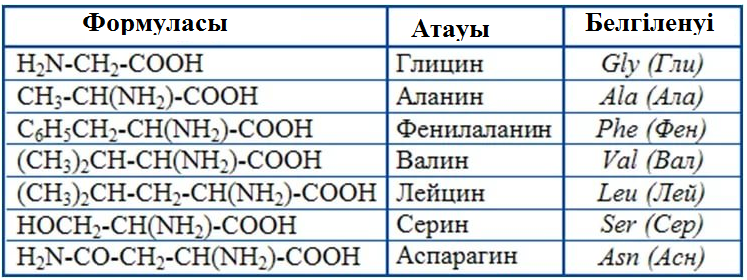
основном тривиальные названия. В природе
встречается свыше 70 аминокислот, но
только 20 из них играют важную роль в
живых системах (таблица 1).
Все
аминокислоты, за исключением пролина
и оксипролина, имеют структуру
R–CH(NΗ2)CO2H;
различия между аминокислотами определяются
природой радикала.
Таблица
1 – Названия аминокислот по различным
номенклатурам
№ | Формула | Название | ||
Тривиальное | Рациональное | Систематическое | ||
1 | NH2–CH2–COOH | Глицин | аминоуксусная | аминоэтановая |
2 | CH3––CHNH2–COOH | Аланин | α-амино-ропионовая | 2-аминопропановая |
3 | NH2–(CH2)2–COOH | β-Аланин | β-амино- пропионовая | 3-аминопропановая |
4 | (CH3)2–(CH)2NH2–COOH | Валин | α-амино- изовалериановая | 2-амино-3-метил-бутановая |
5 | CH3–CH2–CHNH2–COOH | – | α-амино- масляная | 2-аминобутановая |
6 | CH3–CHNH2–CH2–COOH | – | β-амино- масляная | 3-аминобутановая |
7 | NH2–(CH2)3–COOH | – | y-амино- масляная | 4-аминобутановая |
8 | NH2C–(CH3)2–COOH | – | α-амино- изомасляная | 2-амино-2-метил-пропановая |
9 | (CH3)2–CH–CH2–CH(NH2)–COOH | Лейцин | α-амино- изокапроновая | 2-амино-4-метилпентановая |
10 | CH3–CH2–CH(CH3)–CH(NH2)–COOH | Изолейцин (Ile, | α-амино- β-метил-β-этил- пропионовая | 2-амино-3-метилгексановая |
11 | C6H5–CH2–CH(NH2)–COOH | Фенилаланин | α-амино-β-фенил- пропионовая | 2-амино-3-фенилпропановая |
12 | HO–CH2–CH(NH2)–COOH | Серин | α-амино-β-окси-пропионовая | 2-амино-3-оксипропановая |
13 | Пролин | пирролидин-α-карбоновая | пирролидин-2-карбоновая | |
14 | NH–OH–(CH2)2–(CH)2–COOH | Оксипролин | y-оксипирролидин-α-карбоновая | 3-оксипирролидин-2-карбоновая |
15 | Триптофан | α-амино-β-индолил-пропионовая | 2-амино-3-индолил-пропановая | |
16 | CH3–S–(CH2)2–CH(NH2)–COOH | Метионин | α-амино-y-метил-тиомасляная | 2-амино-4-метилтио-бутановая |
17 | COOH–CH2–CH(NH2)–COOH | Аспарагиновая | аминоянтарная | аминобутан-диовая |
18 | NH2–CO–CH2–CH(NH2)–COOH | Аспарагин | ||
19 | COOH–(CH2)2–CH(NH2)–(COOH)2 | Глутаминовая | α-аминоглутаровая | 2-аминопентан-диовая |
20 | NH2–CO–(CH2)2–CH(NH2)–COOH | Глутамин | ||
22 | NH2–(CH2)4–CH(NH2)–COOH | Лизин | α,ε-диамино-капроновая | 2,6-диамино-гексановая |
23 | Аргинин | α-амино- δ-гуанидино-валериановая | 2-амино-5-гуанидино-пентановая | |
24 | Гистидин | α-амино- β-имидазолил-пропионовая | 2-амино-3-имидазолил-пропановая | |
25 | CH3–CH(OH)–CH(NH2)–COOH | Треонин | α-амино-β-окси-масляная | 2-амино-3-оксибутановая |
26 | HO–(C6H4)–CH2–CH(NH2)–COOH | Тирозин | α-амино-β-(n-гидроксифенил)-пропионовая | 2-амино-3-(n-гидроксифенил)-пропановая |
27 | HS–CH2–CH(NH2)–COOH | Цистеин | α-амино-β-тио-пропионовая; α-амино- β-меркапто-пропионовая | 2-амино- 3-меркапто- пропановая |
28 | COOH–CH(NH2)–CH2–S2–CH2–CH(NH2)–COOH | Цистин (Cys-scy) | β,β‘-дитиоди- α-амино- пропионовая | 3,3′-дитио- 2-амино-пропановая |
Изомерия.
Структурная:
Пространственная:
оптическая
Все
природные аминокислоты (кроме глицина),
являются оптически активными веществами
в результате кислотного или щелочного
гидролиза белков). Большинство из
природных α-аминокислот
принадлежит к L-стерическому
ряду. D-аминокислоты
встречаются в составе немногих белков
микроорганизмов (например, в белках
клеточной стенки бактерий сибирской
язвы). С данной особенностью связывают
устойчивость этих бактерий к расщепляющему
действию ферментов человека и животных.
Согласно
номенклатуре (R,
S),
большинство «природных» или L-амино-
кислот имеет S-конфигурацию.
L-Изолейцип
и L-треонин,
содержащие по два хиральных центра в
молекуле, могут быть любыми членами
пары диастереомеров в зависимости от
конфигурации при β-углеродном
атоме.
Получение
аминокислот
Получение
α-аминокислот
Из
природных веществ.
Белки при гидролизе в водных растворах
в присутствии кислоты дают смесь
α-аминокислот,
которые можно выделить и разделить.
Все они оптически активны.Получение
из α-галогенкарбоновых кислот
in
vitro
(аминирование
или аммонолиз, реакция
Геля–Фольгарда–Зелинского).
Реакция
протекает по механизму SN.
Из галогенозамещенных кислот наиболее
доступны α-галогенозамещенные
кислоты, поэтому способ используется
в основном для синтеза α-аминокислот.
Модифицированный
метод синтеза при помощи малонового
эфира
обычно применяется для синтеза
незамещенных кислот:
Галогенуглеводороды
алкилирует ацетиламинмалоновый эфир:
Аминирование
эфиров α-галогензамещённых кислот
(по
Габриэлю)
–
фталимидный
синтез:
Синтез
Штреккера-Зелинского. Получение
Получение
α-аминокислот
из альдегидов (кетонов) путём действия
на них синильной кислоты (или её соли)
и аммиака (или NH4Cl).
Вначале из
альдегида, циановодородной кислоты и
аммиака образуется α-аминонитрил,
который затем гидролизуется в
аминокислоту:
Синтез
α-аминокислот
по Штреккеру сводится к реакции
карбонильного соединения со смесью
хлорида аммония и цианистого натрия.
Это усовершенствование метода Штреккера
предложено Н.Д. Зелинским и Г.Л.
Стадниковым. В результате реакции этих
неорганических веществ образуются
аммиак и цианистый водород — «активные
компоненты» процесса.
Восстановление
оксимов, гидразонов и
других азотсодержащих производных
кислот:
1.7
Получение из нитросоединений
(реакция
Зинина).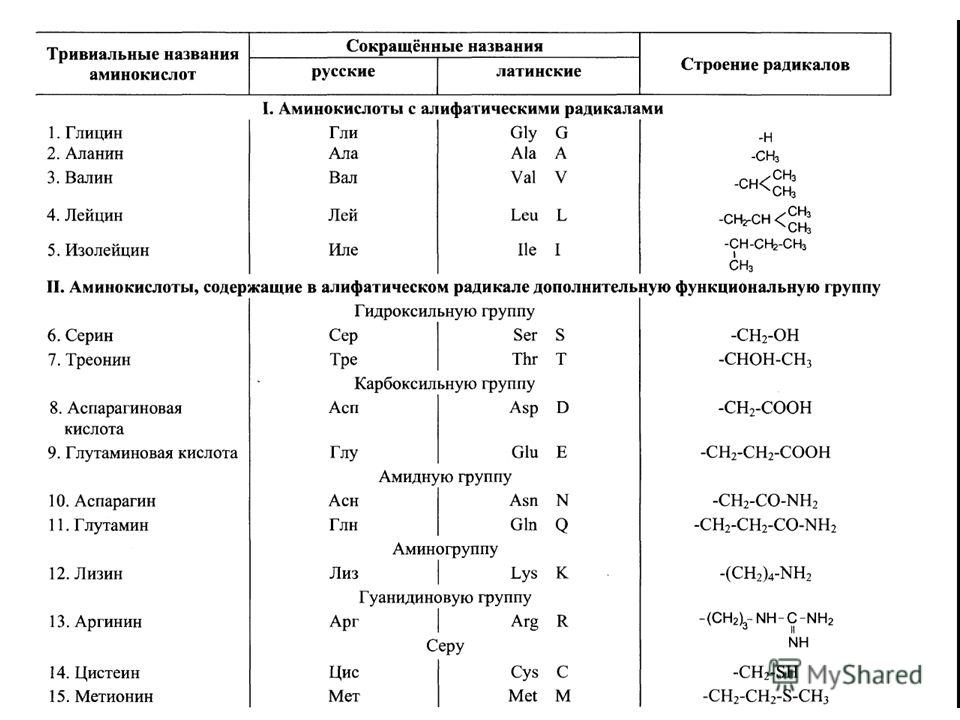
Ароматические аминокислоты получаются
при восстановлении нитропроизводных
ароматических кислот:
Гидролиз
белков.
При гидролизе белков обычно образуются
сложные смеси аминокислот, однако с
помощью специальных хроматографических
методов из этих смесей можно выделять
отдельные чистые аминокислоты. Так из
гидролизатов природных белковых
продуктов получают пролин, цистин,
аргинин, гистидин.
Микробиологический
способ.
Ввиду
сложности химического синтеза и в
связи с трудностями разделения
оптических изомеров некоторые
аминокислоты получают с помощью
микроорганизмов. К таким аминокислотам
относят лизин (пищевой), триптофан,
треонин.
Аминокислоты – общая формула, таблица (химия, 10 класс)
4
Средняя оценка: 4
Всего получено оценок: 790.
4
Средняя оценка: 4
Всего получено оценок: 790.
Органические вещества, в молекуле которых содержатся карбоксильные и аминные группы, называются аминокислотами или аминокарбоновыми кислотами. Это жизненно важные соединения, являющиеся основой построения живых организмов.
Строение
Аминокислота – мономер, состоящий из азота, водорода, углерода и кислорода. Также к аминокислоте могут присоединяться не углеводородные радикалы, например, сера или фосфор.
Условная общая формула аминокислот – NH2-R-COOH, где R – двухвалентный радикал. При этом аминогрупп в одной молекуле может быть несколько.
Рис. 1. Структурное строение аминокислот.
С химической точки зрения аминокислоты – производные карбоновых кислот, в молекуле которых атомы водорода заменены аминогруппами.
Виды
Аминокислоты классифицируются по нескольким признакам. Классификация по трём признакам представлена в таблице.
Признак | Вид | Описание | Пример |
По расположению аминных и карбоксильных групп относительно друг друга | α-аминокислоты | Содержат один атом углерода между функциональными группами | Аланин |
β-, γ-, δ-, ε- и другие аминокислоты | Содержат несколько атомов углерода между функциональными группами | β-аминопропионовая кислота (два атома между группами), ε-аминокапроновая кислота (пять атомов) | |
По изменяемой части (радикалу) | Алифатические (жирные) | Не содержат ароматических связей. | Лизин, серин, треонин, аргинин |
Ароматические | Содержат бензольное кольцо | Фенилаланин, триптофан, тирозин | |
Гетероциклические | Содержат гетероатом – радикал, не являющийся углеродом или водородом | Триптофан, гистидин, пролин | |
Иминокислоты | Содержат иминогруппу NH | Пролин, оксипролин | |
По физико-химическим свойствам | Неполярные (гидрофобные) | Не взаимодействуют с водой | Глицин, валин, лейцин, пролин |
Полярные (гидрофильные) | Взаимодействуют с водой. Подразделяются на незаряженные, положительно и отрицательно заряженные | Лизин, серин, аспартат, глутамат, глутамин |
Рис. 2. Схема классификации аминокислот.
Названия формируются из структурных или тривиальных наименований карбоновых кислот с приставкой «амино-». Цифры показывают, где располагается аминогруппа. Также используются тривиальные названия, заканчивающиеся на «-ин». Например, 2-аминобутановая или α-аминомасляная кислота.
Свойства
Аминокислоты отличаются физическими свойствами от других органических кислот. Все соединения класса – кристаллические вещества, хорошо растворимые в воде, но плохо растворимые в органических растворителях. Они плавятся при высоких температурах, имеют сладковатый вкус и легко образуют соли.
Аминокислоты являются амфотерными соединениями. Благодаря наличию карбоксильной группы -СООН проявляют свойства кислот. Аминогруппа -NH2 обуславливает основные свойства.
Химические свойства соединений:
- горение:
4NH2CH2COOH + 13O2 → 8CO2 + 10H2O + 2N2;
- гидролиз:
NH2CH2COOH + H2O ↔ NH3CH2COOH + OH;
- реакция с раствором щёлочи:
NH2CH2COOH + NaOH → NH2CH2COO-Na + H2O;
- реакция с раствором кислоты:
2NH2CH2COOH + H2SO4 → (NH3CH2COOH)2SO4;
- этерификация:
NH2CH2COOH + C2H5OH → NH2CH2COOC2H5 + H2O.

Из аминокислотных мономеров образуются длинные полимеры – белки. Один белок может включать несколько разных аминокислот. Например, содержащийся в молоке белок казеин состоит из тирозина, лизина, валина, пролина и ряда других аминокислот. В зависимости от строения белки выполняют различные функции в организме.
Рис. 3. Белки.
Что мы узнали?
Из урока химии 10 класса узнали, что такое аминокислоты, какие вещества содержат, как классифицируются. Аминокислоты включают две функциональные группы – аминогруппу -NH2 и карбоксильную группу -COOH. Наличие двух групп обуславливает амфотерность аминокислот: соединения обладают свойствами оснований и кислот. Аминокислоты делятся по нескольким признакам и отличаются количеством аминогрупп, наличием или отсутствием бензольного кольца, присутствием гетероатома, взаимодействием с водой.
Тест по теме
Доска почёта
Чтобы попасть сюда — пройдите тест.
Пока никого нет.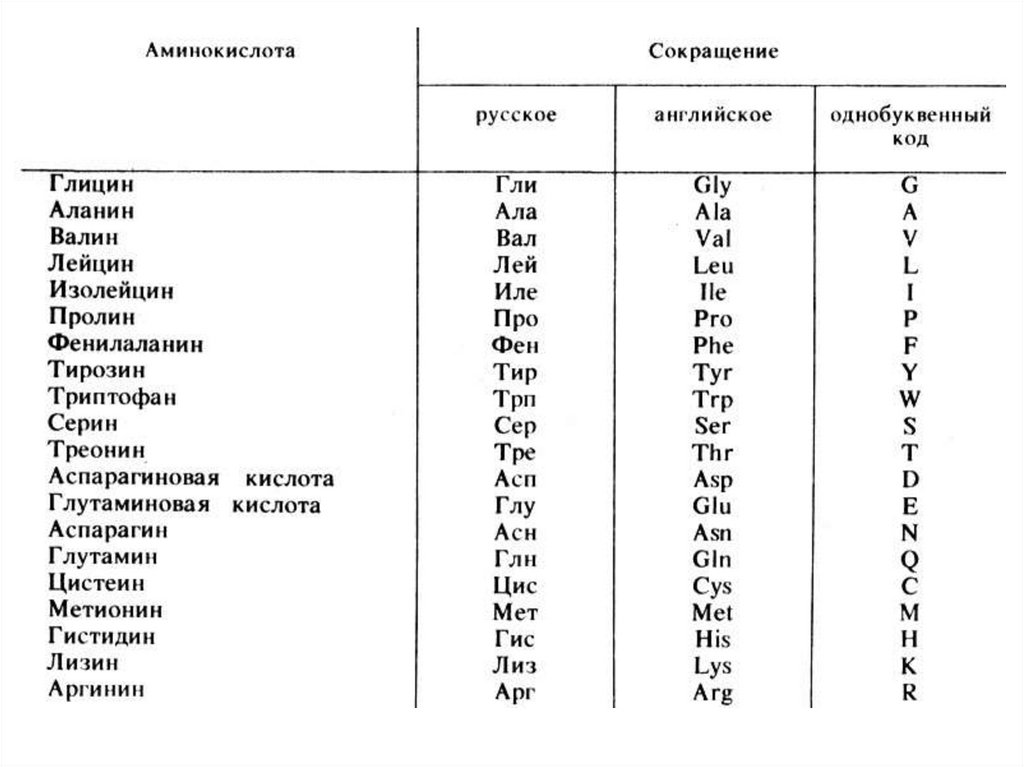 Будьте первым!
Будьте первым!
Оценка доклада
4
Средняя оценка: 4
Всего получено оценок: 790.
А какая ваша оценка?
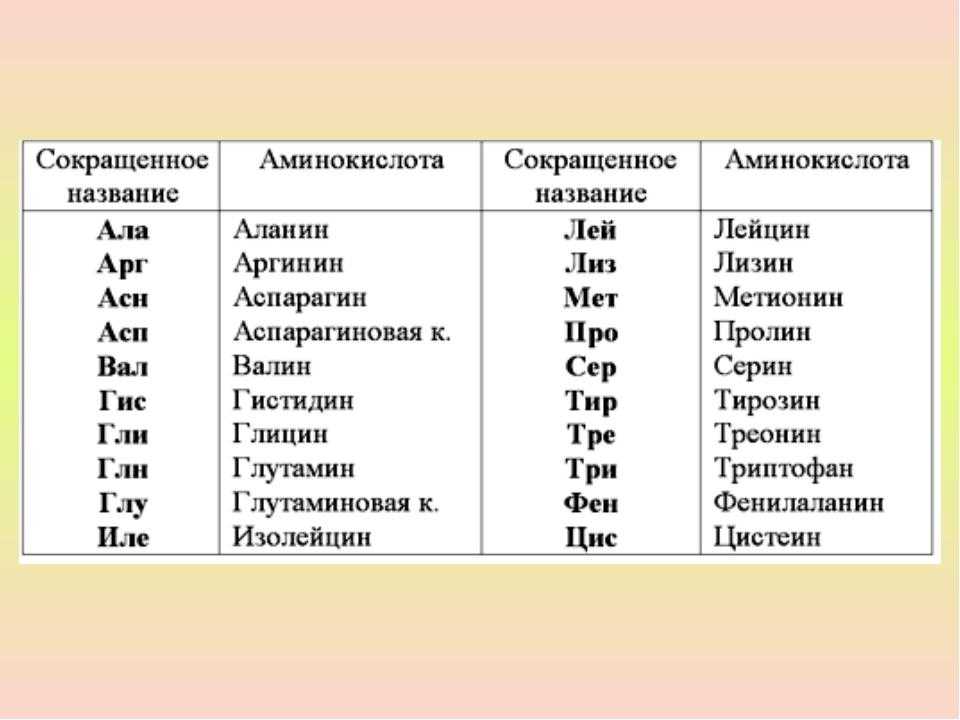
Приложение 4 — Аминокислоты, одно- и трехбуквенные коды
Приложение 4 — Аминокислоты, одно- и трехбуквенные коды
Аминокислота | Трехбуквенный код | Однобуквенный код |
аланин | или | А |
аргинин | аргумент | Р |
аспарагин | как | Н |
аспарагиновая кислота | асп | Д |
аспарагин или аспарагиновая кислота | asx | Б |
цистеин | сис | С |
глутаминовая кислота | клей | Е |
глютамин | Глн | В |
глутамин или глутаминовая кислота | глик | З |
глицин | гли | Г |
гистидин | его | Х |
изолейцин | или | я |
лейцин | лей | л |
лизин | лс | К |
метионин | с | М |
фенилаланин | фэ | Ф |
пролин | про | Р |
серин | сер | С |
треонин | через | Т |
триптофан | тп | Вт |
тирозин | тыр | Д |
валин | знач | В |
Коды, используемые в описании последовательности
Аннотированные/собранные последовательности DDBJ
Нуклеотид
Базовые коды нуклеотидов
Коды оснований нуклеотидов, которые используются с Международным
База данных нуклеотидных последовательностей выглядит следующим образом.
Данные последовательности выражаются только строчными буквами. Заглавная буква будет
быть автоматически преобразованы в строчные буквы.
| Символ | Значение | Пояснение |
|---|---|---|
| и | и | аденин |
| с | с | цитозин |
| г | г | гуанин |
| т | т | тимин в ДНК; урацил в РНК |
| м | а или с | амино |
| р | а или г | пурин |
| с | а или т | |
| с | к или г | |
| у | с или т | пиримидин |
| к | г или т | кето |
| v | а или в или г | не т |
| ч | а или с или т | не г |
| д | а или г или т | не с |
| б | с или г или т | а не |
| п | а или в или г или т | любой |
[Ссылки]
- Cornish-Bowden, A.
 Nucl Acid Res 13, 3021-3030 (1985)
Nucl Acid Res 13, 3021-3030 (1985) - Определение таблицы характеристик: 7.4.1
Коды оснований нуклеотидов (IUPAC)
Модифицированные базовые сокращения
Пример описания модифицированной базы в строке FEATURES.
Пример
ОСОБЕННОСТИ Место/Квалификаторы
модифицированная_база 15
/mod_base="m2g"
| Сокращение | Модифицированное базовое описание |
|---|---|
| ак4с | 4-ацетилцитидин |
| чм5у | 5-(карбоксигидроксиметил)уридин |
| см | 2’-О-метилцитидин |
| смнм5с2у | 5-карбоксиметиламинометил-2-тиуридин |
| смнм5у | 5-карбоксиметиламинометилуридин |
| зху | дигидроуридин |
| фм | 2’-O-метилпсевдоуридин |
| галлон q | бета, D-галактозилкевозин |
| г | 2’-O-метилгуанозин |
| и | инозин |
| и6а | N6-изопентениладенозина |
| м1а | 1-метиладенозин |
| м1ф | 1-метилпсевдоуридин |
| м1г | 1-метилгуанозин |
| м1и | 1-метилинозин |
| м22г | 2,2-диметилгуанозин |
| м2а | 2-метиладенозин |
| м2г | 2-метилгуанозин |
| м3с | 3-метилцитидин |
| м4с | N4-метилцитозин |
| м5с | 5-метилцитидин |
| м6а | N6-метиладенозин |
| м7г | 7-метилгуанозин |
| мам5у | 5-метиламинометилуридин |
| мам5с2у | 5-метоксиаминометил-2-тиуридин |
| человек q | бета, D-маннозилкевозин |
| мкм5с2у | 5-метоксикарбонилметил-2-тиуридин |
| мкм5у | 5-метоксикарбонилметилуридин |
| мо5у | 5-метоксиуридин |
| мс2и6а | 2-метилтио-N6-изопентениладенозина |
| мс2т6а | N-((9-бета-D-рибофуранозил-2-метилтиопурин-6-ил)карбамоил)треонин |
| мт6а | N-((9-бета-D-рибофуранозилпурин-6-ил)N-метилкарбамоил)треонин |
| мв | Метиловый эфир уридин-5-оксиуксусной кислоты |
| о5у | уридин-5-оксиуксусная кислота (v) |
| osyw | вибутоксозин |
| р | псевдоуридин |
| к | кеуозин |
| с2к | 2-тиоцитидин |
| с2т | 5-метил-2-тиуридин |
| с2у | 2-тиуридин |
| с4у | 4-тиуридин |
| м5у | 5-метилуридин |
| т6а | N-((9-бета-D-рибофуранозилпурин-6-ил)карбамоил)треонин |
| тм | 2’-О-метил-5-метилуридин |
| мм | 2’-O-метилуридин |
| гв | вибутозин |
| х | 3-(3-амино-3-карбоксипропил)уридин, (acp3)u |
| ДРУГОЕ | Другое (/примечание квалификатор に修飾塩基を記載します) |
[Ссылки]
- Sprinzl, M.
 and Gauss, D.H. Nucl Acid Res 10, r1 (1982). (обратите внимание, что
and Gauss, D.H. Nucl Acid Res 10, r1 (1982). (обратите внимание, что
в Cornish_Bowden, A. Nucl Acid Res 13, 3021-3030 (1985)
IUPAC-IUB отказался рекомендовать набор сокращений для модифицированных
нуклеотидов) - Определение таблицы характеристик: 7.4.2 Изменено
базовые сокращения
Аминокислота
Коды аминокислот
Код аминокислоты, который используется с Международным кодом нуклеотидов.
База данных последовательностей выглядит следующим образом.
Эти аминокислоты обозначаются однобуквенной аббревиатурой в
/translation квалификатор CDS
особенность.
Перечисленные аббревиатуры аминокислот являются допустимыми значениями для квалификаторов.
/transl_кроме и
/антикодон.
Те, которые не включены в «Коды аминокислот», см.
Модифицированные и необычные аминокислоты.
| Сокращение | Однобуквенное сокращение | Название аминокислоты |
|---|---|---|
| Аля | А | Аланин |
| Аргумент | Р | Аргинин |
| Асн | Н | Аспарагин |
| Асп | Д | Кислота аспарагиновая |
| Цис | С | Цистеин |
| Глн | В | Глютамин |
| Клей | Е | Глутаминовая кислота |
| Гли | Г | Глицин |
| Его | Х | Гистидин |
| Иль | я | Изолейцин |
| Лев | л | Лейцин |
| Лис | К | Лизин |
| Мет | М | Метионин |
| Фе | Ф | Фенилаланин |
| Про | Р | Пролайн |
| Пыл | О | Пирролизин |
| Серия | С | Серин |
| сек | У | Селеноцистеин |
| Через | Т | Треонин |
| Трп | Вт | Триптофан |
| Тыр | Д | Тирозин |
| Вал | В | Валин |
| Асх | Б | Аспарагиновая кислота или аспарагин |
| Глюкс | З | Глутаминовая кислота или глутамин |
| Хаа | х | Любая аминокислота |
| Шле | Дж | Лейцин или изолейцин |
| СРОК | терминирующий кодон |
[Ссылки]
- Совместная комиссия IUPAC-IUB по биохимической номенклатуре.
 Номенклатура
Номенклатура
и символизм аминокислот и пептидов. Евро. Дж. Биохим. 138:
9-37 (1984). - Определение таблицы функций: 7.4.3 Amino
кислотные сокращения
Модифицированные и необычные аминокислоты
Для других аминокислот, не входящих в состав Amino Acid
Коды, используются приведенные ниже аббревиатуры. Все эти амино
кислоты обозначаются однобуквенной аббревиатурой «Х» в
/translation квалификатор CDS
особенность.
| Сокращение | Название аминокислоты |
|---|---|
| Аад | 2-аминоадипиновая кислота |
| БАД | 3-Аминоадипиновая кислота |
| бала | бета-аланин, бета-аминопропионовая кислота |
| Абу | 2-аминомасляная кислота |
| 4Абу | 4-аминомасляная кислота, пиперидиновая кислота |
| Акп | 6-аминокапроновая кислота |
| Ахэ | 2-Аминогептановая кислота |
| Аиб | 2-аминоизомасляная кислота |
| бАиб | 3-аминоизомасляная кислота |
| Апм | 2-аминопимелиновая кислота |
| Дбу | 2,4-диаминомасляная кислота |
| Des | Десмозин |
| ДПМ | 2,2’-диаминопимелиновая кислота |
| Дпр | 2,3-Диаминопропионовая кислота |
| ЭтГли | N-этилглицин |
| ЭтАсн | N-этиласпарагин |
| Хил | Гидроксилизин |
| ахил | алло-гидроксилизин |
| 3Hyp | 3-гидроксипролин |
| 4Hyp | 4-гидроксипролин |
| Иде | Изодесмозин |
подв. |


 Получение
Получение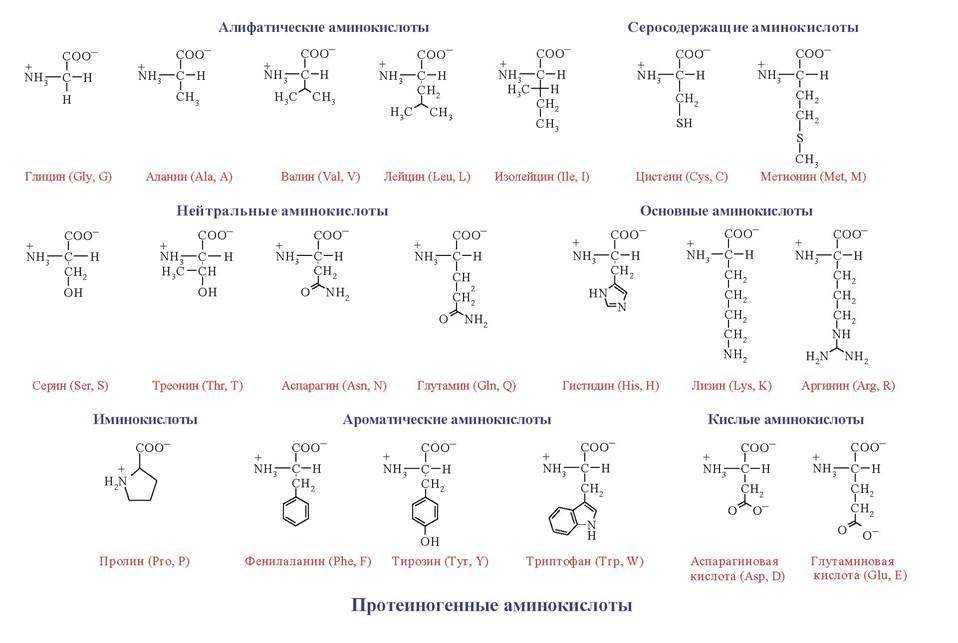 Бывают линейными и циклическими
Бывают линейными и циклическими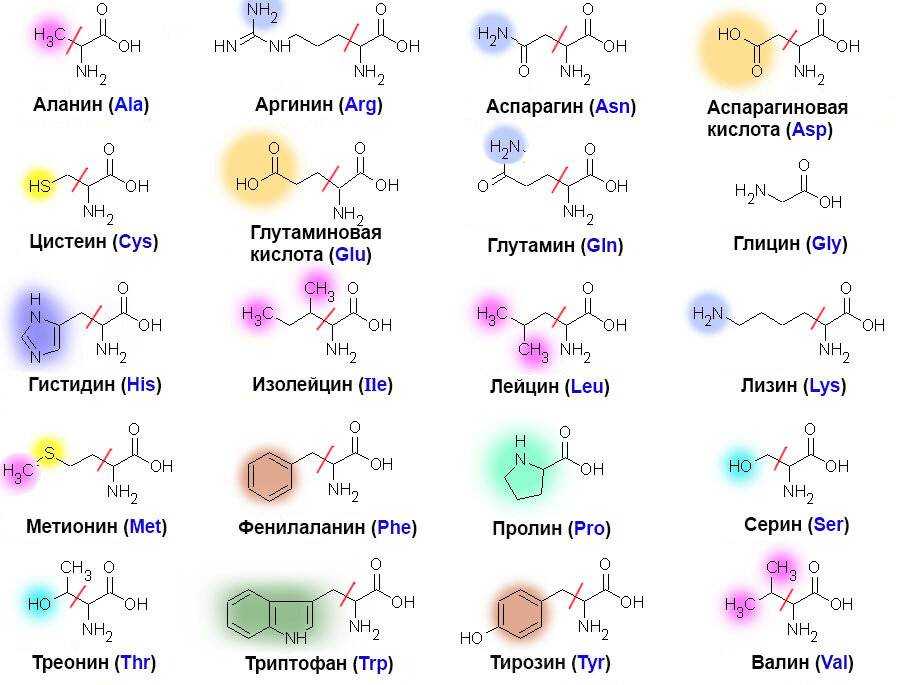
 Nucl Acid Res 13, 3021-3030 (1985)
Nucl Acid Res 13, 3021-3030 (1985) and Gauss, D.H. Nucl Acid Res 10, r1 (1982). (обратите внимание, что
and Gauss, D.H. Nucl Acid Res 10, r1 (1982). (обратите внимание, что Номенклатура
Номенклатура